
Wetenschap
Welke ionen zullen de zuren en basen in water vormen?
Zuren:
- Sterke zuren, zoals zoutzuur (HCl) en zwavelzuur (H2SO4), dissociëren volledig in water, waarbij waterstofionen (H+) en de overeenkomstige anionen vrijkomen. Bijvoorbeeld:
```
HCl(aq) → H+(aq) + Cl-(aq)
```
- Zwakke zuren, zoals azijnzuur (CH3COOH), dissociëren gedeeltelijk in water, waardoor een evenwicht ontstaat tussen het niet-gedissocieerde zuur en de ionen. Bijvoorbeeld:
```
CH3COOH(aq) ⇌ H+(aq) + CH3COO-(aq)
```
Basis:
- Sterke basen, zoals natriumhydroxide (NaOH) en kaliumhydroxide (KOH), dissociëren volledig in water, waarbij hydroxide-ionen (OH-) en de overeenkomstige kationen vrijkomen. Bijvoorbeeld:
```
NaOH(aq) → Na+(aq) + OH-(aq)
```
- Zwakke basen, zoals ammoniak (NH3), dissociëren gedeeltelijk in water, waardoor een evenwicht ontstaat tussen de niet-gedissocieerde base en de ionen. Bijvoorbeeld:
```
NH3(aq) + H2O(l) ⇌ NH4+(aq) + OH-(aq)
```
Samenvattend geven zuren H+-ionen af wanneer ze in water worden opgelost, terwijl basen OH-ionen afgeven. De sterkte van een zuur of base bepaalt de mate van ionisatie en de concentratie van de resulterende ionen in oplossing.
 Platina heeft een dichtheid van 21 g/cm3. Een platinaring wordt in een maatcilinder geplaatst die water bevat. Het waterniveau stijgt van 5,0 ml naar 5,3 wanneer het wordt toegevoegd. Welke massaring?
Platina heeft een dichtheid van 21 g/cm3. Een platinaring wordt in een maatcilinder geplaatst die water bevat. Het waterniveau stijgt van 5,0 ml naar 5,3 wanneer het wordt toegevoegd. Welke massaring?  Nabij-infrarood reflecterende mengcoatings hebben betere optische en koelprestaties
Nabij-infrarood reflecterende mengcoatings hebben betere optische en koelprestaties Hoeveel moleculen zijn er aanwezig in 1 molaire massa zwavelzuur?
Hoeveel moleculen zijn er aanwezig in 1 molaire massa zwavelzuur?  Wat is universeel pH-papier?
Wat is universeel pH-papier?  Marine bacterieel exopolysaccharide EPS11 remt migratie en invasie van leverkankercellen
Marine bacterieel exopolysaccharide EPS11 remt migratie en invasie van leverkankercellen
Hoofdlijnen
- Who Discovered Ribosomes Structure?
- Hoe een stedelijke vleermuis verschilt van een landelijke vleermuis
- Een schakelaar voor de interne klok:onderzoek naar kwantumbiologie voor nieuwe medische therapieën
- Nieuwe studie onderzoekt ATP-synthase in zure toestand om te onthullen hoe het enzym functioneert
- Wetenschappers ontcijferen mechanismen die ten grondslag liggen aan de biologie van veroudering
- Zelfs als je nog niet weet dat je ziek bent, je gezicht zal je verraden
- Wetenschappers introduceren DIProT:een interactieve deep learning-toolkit voor efficiënt eiwitontwerp
- Een wiskundig principe legt uit hoe cellen zich met elkaar verbinden om weefsels en organen te vormen
- Wat is de definitie van lipofiel?
- Voedingswetenschappers creëren nieuwe magnetische nanodeeltjes voor snelle screening van bestrijdingsmiddelenresiduen in groenten

- Middeleeuwse kruitrecepten opblazen

- Nieuwe technologie zet afvalplastic in een uur om in vliegtuigbrandstof

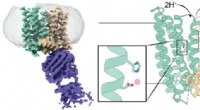
- Onthulling van de onverwachte structuur van ijzer-exporteur ferroportine
- Een materiaal ondersteboven keren kan het soms zachter maken

 Liefhebbers en leugenaars:hoeveel sekspartners heb je werkelijk gehad?
Liefhebbers en leugenaars:hoeveel sekspartners heb je werkelijk gehad?  Regen speelt een verrassende rol bij het gezonder maken van sommige herstelde prairies dan andere
Regen speelt een verrassende rol bij het gezonder maken van sommige herstelde prairies dan andere Wat gebeurt er met een kooktemperatuur als de druk afneemt?
Wat gebeurt er met een kooktemperatuur als de druk afneemt?  Extreme hitte en ozonvervuiling:een oproep voor gerichte controlestrategieën in China
Extreme hitte en ozonvervuiling:een oproep voor gerichte controlestrategieën in China  Analytisch model voorspelt precies hoeveel een stuk hardware datacenters zal versnellen
Analytisch model voorspelt precies hoeveel een stuk hardware datacenters zal versnellen Hoe een bio-bot te bouwen:Onderzoekers delen het ontwerp en de ontwikkeling van biologische machines
Hoe een bio-bot te bouwen:Onderzoekers delen het ontwerp en de ontwikkeling van biologische machines  Hoe foto-elektroden veranderen in contact met water
Hoe foto-elektroden veranderen in contact met water  Welk deel van een plant vertoont een duidelijke groei?
Welk deel van een plant vertoont een duidelijke groei?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

