
Wetenschap
Gebruik Lewis-structuren en vsepr-theorie om te bepalen welke ch4 ch3cl polair niet-polair zijn?
* Lewis-structuur:H-C-H
* VSEPR-vorm:tetraëdrisch
* Polariteit:niet-polair
CH₃Cl
* Lewis-structuur:H-C-Cl
* VSEPR-vorm:tetraëdrisch
* Polariteit:polair
Uitleg:
In CH₄ zijn de vier waterstofatomen symmetrisch rond het koolstofatoom gerangschikt. Dit betekent dat de elektronegativiteit van de waterstofatomen teniet wordt gedaan en dat het molecuul niet-polair is.
In CH₃Cl is het chlooratoom elektronegatiever dan de waterstofatomen. Dit betekent dat de elektronen in de C-Cl-binding naar het chlooratoom worden getrokken, waardoor een polaire binding ontstaat. Het molecuul als geheel is ook polair, omdat het positieve uiteinde van de C-Cl-binding dichter bij het chlooratoom ligt dan het negatieve uiteinde.
 Nieuwe supramoleculaire copolymeren aangedreven door zelfsortering van moleculen
Nieuwe supramoleculaire copolymeren aangedreven door zelfsortering van moleculen Onderzoeksvoortgang van gelaagde, op dubbele hydroxide gebaseerde elektrokatalysator voor watersplitsing
Onderzoeksvoortgang van gelaagde, op dubbele hydroxide gebaseerde elektrokatalysator voor watersplitsing  Hoe de dikke darm prioriteit geeft aan gasontgifting boven energieverbruik?
Hoe de dikke darm prioriteit geeft aan gasontgifting boven energieverbruik? Een complete set van energieniveauposities van alle primaire metaalhalogenideperovskieten
Een complete set van energieniveauposities van alle primaire metaalhalogenideperovskieten Maakt platina deel uit van de platinafamilie?
Maakt platina deel uit van de platinafamilie?
 Onderzoek toont aan dat bosbranden ooit het uitsterven van Zuid-Californië hebben aangewakkerd; zal het weer gebeuren?
Onderzoek toont aan dat bosbranden ooit het uitsterven van Zuid-Californië hebben aangewakkerd; zal het weer gebeuren?  Wetenschappers verbeteren de timing van mistwaarschuwingen door veranderingen in het elektrische veld in de atmosfeer te detecteren
Wetenschappers verbeteren de timing van mistwaarschuwingen door veranderingen in het elektrische veld in de atmosfeer te detecteren  Zuid-Afrikaanse gemeenschappen versus Shell:overwinningen bij het Hooggerechtshof laten zien dat culturele overtuigingen en praktijken meetellen in klimaatzaken
Zuid-Afrikaanse gemeenschappen versus Shell:overwinningen bij het Hooggerechtshof laten zien dat culturele overtuigingen en praktijken meetellen in klimaatzaken  Onderzoek toont aan hoe natuurlijke verstoringen de reactiestrategieën op klimaatverandering beïnvloeden
Onderzoek toont aan hoe natuurlijke verstoringen de reactiestrategieën op klimaatverandering beïnvloeden  Ze kunnen meer koolstof vastleggen dan ze uitstoten. Dus waarom zijn houten gebouwen niet mainstream?
Ze kunnen meer koolstof vastleggen dan ze uitstoten. Dus waarom zijn houten gebouwen niet mainstream?
Hoofdlijnen
- Kwallen, geen kaken:onderzoek onthult waar we het meest bang voor zijn in de oceaan
- Een duidelijker beeld van hoe huurmoordenaars zich ontwikkelden
- Waarom DNA de meest gunstige moleculen is voor genetisch materiaal en hoe RNA zich verhoudt tot deze Respect
- Hoe plantrottende bacteriën ijzer stelen om te overleven
- Wat doodde tonnen vissen in de Europese rivier? Het mysterie wordt dieper
- Hoe kan embryonale ontwikkeling worden gebruikt als bewijs voor evolutie?
- Chemici, biologen, archeologen:wie zal de recepten van onze voorouders opgraven?
- Wat is een positieve controle in de microbiologie?
- Waarom zijn cellen belangrijk voor levende organismen?
- De weg vrijmaken voor kunstmatige fotosynthese:effect van doping op de fotokatalysator SrTiO3

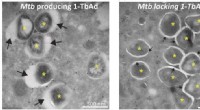
- Antacida helpt tuberculosebacteriën te overleven
- Neutronen en röntgenstralen gebruiken om de veroudering van lithiumbatterijen te analyseren

- Gezamenlijk onderzoek kan leiden tot verbeteringen in de productie van koolstofvezels

- Zonne-energie omzetten in waterstofbrandstof, met hulp van fotosynthese

 Nieuwe technieken laten zien hoe microben de gezondheid en biodiversiteit van oceanen bepalen
Nieuwe technieken laten zien hoe microben de gezondheid en biodiversiteit van oceanen bepalen  NASA vindt zware regenval in intensivering van tropische storm Harvey
NASA vindt zware regenval in intensivering van tropische storm Harvey Onderzoekers gebruiken lichtgevoelige moleculen om eiwitten te volgen die cruciaal zijn voor celsignalering
Onderzoekers gebruiken lichtgevoelige moleculen om eiwitten te volgen die cruciaal zijn voor celsignalering Hoe atoomklokken werken
Hoe atoomklokken werken  Nieuw nanomateriaal, in de vorm van Davidssterren, ontdekt door Israëlische wetenschappers
Nieuw nanomateriaal, in de vorm van Davidssterren, ontdekt door Israëlische wetenschappers Droidbugs:een nieuwe benchmark om geautomatiseerde reparatiemethoden voor Android-apps te evalueren
Droidbugs:een nieuwe benchmark om geautomatiseerde reparatiemethoden voor Android-apps te evalueren In dating-apps, stelt het vrouwen echt in staat hen te dwingen de eerste stap te zetten?
In dating-apps, stelt het vrouwen echt in staat hen te dwingen de eerste stap te zetten? Onderzoekers ontdekken nieuwe optische detectietechnologie
Onderzoekers ontdekken nieuwe optische detectietechnologie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

