
Wetenschap
Opheldering van de moleculaire doelen van eicosapentaeenzuur:een natuurlijke remedie tegen chronische pijn
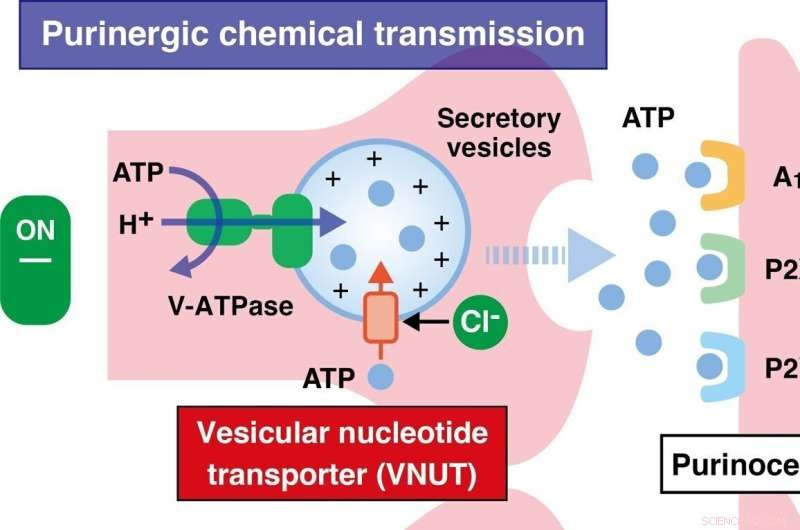
Nieuwe studie identificeert vesiculaire nucleotide transporter als een nieuw doelwit van eicosapentaeenzuur (EPA) en benadrukt het mechanisme dat ten grondslag ligt aan het analgetische effect van EPA. EPA vermindert krachtig neuropathische en inflammatoire pijn en insulineresistentie, met minder bijwerkingen. Krediet:Takaaki Miyaji van de universiteit van Okayama
Eicosapentaeenzuur (EPA) is een essentiële voedingsstof die behoort tot de omega-3-groep van meervoudig onverzadigde vetzuren (PUFA's). Aangezien het menselijk lichaam geen PUFA's kan synthetiseren, zijn voedingssupplementen die EPA bevatten vereist voor normale fysiologische functies. Overvloedig gevonden in natuurlijke bronnen zoals vis, hennepolie en lijnzaadolie, is bekend dat EPA ontstekingsremmende, neuroprotectieve en cardiovasculaire beschermende activiteiten vertoont.
Bovendien hebben recente studies de therapeutische effecten ervan aangetoond bij het verminderen van het sterfterisico na een myocardinfarct, het verbeteren van de insulineresistentie, het verlagen van de bloedlipideniveaus en het remmen van de bloedplaatjesaggregatie. Van omega-3 PUFA's is ook aangetoond dat ze de ontstekingsreacties verminderen na een COVID-19-infectie. Ondanks het brede spectrum van zijn therapeutische effecten, blijven de moleculaire doelwitten en het onderliggende mechanisme van de werking van EPA ongrijpbaar.
Onderzoeksprofessor Takaaki Miyaji van de Okayama University, Japan, en zijn team van onderzoekers hebben nu een nieuw moleculair doelwit van EPA ontdekt in hun recente werk gepubliceerd in het tijdschrift Proceedings of the National Academy of Sciences .
Onderzoeksprofessor Miyaji, de corresponderende auteur van dit artikel, verklaart de grondgedachte achter hun studie en zegt dat "conventionele moleculaire doelwitten zoals COX-2-remmers de ontstekingsremmende en analgetische effecten kunnen verklaren voor ontstekingspijn, maar niet voor neuropathische pijn, van EPA Omdat EPA echter zowel inflammatoire als neuropathische pijn aanzienlijk verzacht, is er een sterke mogelijkheid dat er een ander belangrijk moleculair doelwit van EPA bestaat dat verband houdt met neuropathie." Door dieper te duiken, probeerde het team het werkingsmechanisme van EPA te begrijpen bij het verlichten van zowel inflammatoire als neuropathische pijn.
Tijdens neurologische, metabolische en immunologische verstoringen leidt "purinerge" chemische transmissie (een vorm van extracellulaire signalering gemedieerd door purinederivaten) tot de binding van energiedragers zoals adenosinetrifosfaat (ATP) aan "purinoreceptoren", wat neuropathische en inflammatoire pijn perceptie. Deze binding wordt gemedieerd door een vesiculaire nucleotidetransporter (VNUT), die zo het sleutelmolecuul wordt bij de initiatie van purinerge signalering. De onderzoekers veronderstelden dat EPA zich richt op VNUT, waardoor de purinerge chemische transmissie wordt geblokkeerd en de pijnperceptie wordt verminderd.
Onderzoeksprofessor Miyaji en zijn team testten deze hypothese zowel in vitro, met behulp van van de mens afgeleide VNUT, als in vivo, met behulp van een VNUT-deficiënt muismodel.
Ze ontdekten dat EPA concurreert met chloorionen die normaal VNUT activeren en de door VNUT gemedieerde afgifte van ATP remt. Bovendien zagen ze dit effect alleen met EPA en zijn metabolieten, en niet met docosahexaeenzuur, een ander omega-3 vetzuur, wat suggereert dat de structuur van omega-3 vetzuren met zijketens noodzakelijk is voor VNUT-remming.
Verder induceerden ze neuropathische pijn bij wildtype en VNUT-deficiënte muizen met behulp van chemotherapeutische middelen die worden gebruikt bij de behandeling van kanker. EPA accentueerde met name pijn bij wildtype dieren, maar niet bij VNUT-deficiënte muizen, waardoor hun eerdere bevinding over het remmende effect van EPA op VNUT wordt bevestigd. Evenzo is aangetoond dat insulineresistentie, veroorzaakt door neuropathische pijn, wordt verminderd door EPA-behandeling bij wildtype, maar niet bij VNUT-deficiënte muizen.
"We ontdekten dat lage concentraties EPA de afgifte van ATP uit neuronen volledig en omkeerbaar remden, zonder de afgifte van andere neurotransmitters te remmen. Vergeleken met andere geneesmiddelen vertoonde EPA een hoger analgetisch effect en minder bijwerkingen", legt onderzoeksprofessor Miyaji uit.
Naast neuropathische pijn en bijbehorende insulineresistentie, kunnen de analgetische effecten van EPA verder worden uitgebreid tot chronische pijn geassocieerd met verschillende andere aandoeningen zoals chemotherapie, diabetes, reuma, jicht, heupzenuwligatie en ontsteking. Bovendien wordt purinerge chemische transmissie ook geassocieerd met een verscheidenheid aan aandoeningen, waaronder de ziekte van Alzheimer en depressie, waarvoor EPA kan worden onderzocht als een therapeutische strategie.
Bovendien kunnen opioïden en andere pijnstillers langdurige bijwerkingen hebben en tot verslavingen leiden. Bij gebrek aan optimale medicamenteuze behandelingen met minder bijwerkingen, leidt chronische pijn tot een verminderde kwaliteit van leven, naast een toename van de economische last van de behandeling. Met deze ontdekking kunnen 'op voedingsstoffen gebaseerde EPA' en zijn metabolieten worden geïndiceerd bij de behandeling van chronische pijn, terwijl ook mogelijke bijwerkingen op afstand worden gehouden.
Onderzoeksprofessor Miyaji, die de langetermijnimplicaties van hun onderzoek uitwerkt, voegt eraan toe dat hun "resultaten kunnen helpen bij het ontwikkelen van nieuwe op voedingsstoffen gebaseerde behandelings- en preventiestrategieën door zich te richten op purinerge chemische overdracht van ontstekings-, neurologische en metabole ziekten, zonder de nadelige bijwerkingen van conventionele pijnstillende medicijnen." + Verder verkennen
Potentieel medicijn voor de behandeling van chronische pijn met weinig bijwerkingen
 Het bereiken van stabiele K-opslagprestaties van met koolstofbolletjes opgesloten antimoon via elektrolytregulatie
Het bereiken van stabiele K-opslagprestaties van met koolstofbolletjes opgesloten antimoon via elektrolytregulatie Fysieke en chemische eigenschappen voor het Element Aluminium
Fysieke en chemische eigenschappen voor het Element Aluminium Verschillende manieren om ijsblokjes te smelten
Verschillende manieren om ijsblokjes te smelten IJsvorming op oppervlakken versterkt via een niet-klassiek kiemvormingsproces
IJsvorming op oppervlakken versterkt via een niet-klassiek kiemvormingsproces Science Fair-projecten op kauwgom
Science Fair-projecten op kauwgom
 Dankzij klimaatverandering en natter weer, bosbodems nemen minder methaan op
Dankzij klimaatverandering en natter weer, bosbodems nemen minder methaan op Tientallen gevreesde doden in hittegolf Karachi:liefdadigheid
Tientallen gevreesde doden in hittegolf Karachi:liefdadigheid Riffen sterven af. Wetenschappers hopen dat in het laboratorium gekweekte superkoralen hen kunnen helpen om ze nieuw leven in te blazen
Riffen sterven af. Wetenschappers hopen dat in het laboratorium gekweekte superkoralen hen kunnen helpen om ze nieuw leven in te blazen Franse rechtbank behandelt historische zaak over inactiviteit van klimaat
Franse rechtbank behandelt historische zaak over inactiviteit van klimaat Hoe maak je je eigen weerkaart
Hoe maak je je eigen weerkaart
Hoofdlijnen
- Bewaken van genetische mutaties die belangrijk zijn voor panterbeheer in Florida
- Fysieke aanpassingen van rondwormen
- Wat is de subeenheid van DNA genaamd?
- Hoe krijgen mensen zuurstof in hun lichaam?
- Onderzoek onthult een nieuwe overlevingsstrategie in belangrijke bacteriën
- Een bijtend rapport:onderzoek toont aan dat klimaatverandering een grote bedreiging vormt voor hommels
- De celstructuur van een ui
- Wat is het verschil tussen een gedupliceerd chromosoom en een chromaat?
- Een dodelijke ziekte heeft zeven Australische kikkersoorten met uitsterven gedreven. Maar deze bedreigde kikker vecht terug
- Nieuwe techniek om de productie van farmaceutische verbindingen te automatiseren

- Materiaalwetenschappers verdiepen zich in kwetsbaarheden die betrokken zijn bij tandbederf bij de mens
- Moleculen zetten zichtbaar licht om in ultraviolet licht met een recordrendement

- Hechtgedrag van zelfconstructieve materialen voor het eerst gemeten
- Haar vindt nieuwe wortels als groeimedium voor stadslandbouw

 Met lava gevulde blokken op Venus kunnen wijzen op geologische activiteit
Met lava gevulde blokken op Venus kunnen wijzen op geologische activiteit Onderzoekers observeren voor het eerst ultrasnelle processen van afzonderlijke moleculen
Onderzoekers observeren voor het eerst ultrasnelle processen van afzonderlijke moleculen Afbeelding:Hubbles merkwaardig geval van een calciumrijke supernova
Afbeelding:Hubbles merkwaardig geval van een calciumrijke supernova Wetenschappers onderzoeken de kracht van radiogolven om fusiereacties onder controle te houden
Wetenschappers onderzoeken de kracht van radiogolven om fusiereacties onder controle te houden Waar zal Amazon zijn tweede hoofdkantoor vestigen? Wat je moet weten
Waar zal Amazon zijn tweede hoofdkantoor vestigen? Wat je moet weten COVID-19 stelt nieuwe wetenschap op de proef
COVID-19 stelt nieuwe wetenschap op de proef Op hydrogel gebaseerde capsules kunnen dagenlang uitzetten en in het maagdarmkanaal blijven, langzaam medicatie afgeven
Op hydrogel gebaseerde capsules kunnen dagenlang uitzetten en in het maagdarmkanaal blijven, langzaam medicatie afgeven Apps kunnen binnenkort uw levensverwachting voorspellen, maar wil je het weten?
Apps kunnen binnenkort uw levensverwachting voorspellen, maar wil je het weten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

