
Wetenschap
Welk systeem handhaaft de pH van menselijk bloed?
Hier is hoe het werkt:
* Koolstofdioxide (CO2) is een afvalproduct van het metabolisme en lost op in bloed. Deze opgeloste CO2 reageert met water om koolzuur te vormen (H2CO3).
* koolzuur is een zwak zuur dat kan dissociëren in waterstofionen (H+) en bicarbonaationen (HCO3-)
* De balans tussen koolzuur en bicarbonaationen is cruciaal voor het handhaven van de pH van het bloed.
Hier is een vereenvoudigde uitsplitsing:
* Wanneer bloed te zuur wordt (lage pH): De bicarbonaationen (HCO3-) reageren met de overtollige waterstofionen (H+) om koolzuurzuur (H2CO3) te vormen, die vervolgens afbreekt in water en CO2. Dit proces verwijdert overtollige H+ -ionen, waardoor de pH weer normaal wordt.
* Wanneer bloed te basic wordt (hoge pH): Koolzuurzuur (H2CO3) dissocieert, waardoor waterstofionen (H+) in het bloed worden vrijgeeft. Dit verhoogt de zuurgraad van het bloed, waardoor de pH weer normaal wordt verlaagd.
De nieren spelen ook een rol bij het handhaven van de pH van de bloed:
* Ze scheiden overtollige zuur of base uit in de urine. Dit helpt de bicarbonaationconcentratie in het bloed aan te passen, wat verder bijdraagt aan pH -regulering.
Het bicarbonaatbuffersysteem, samen met de nieren, werkt samen om de bloed -pH binnen een smal bereik te houden (7,35 tot 7,45), wat essentieel is voor de juiste lichamelijke functie.
 Hoe beschrijven wetenschappers de aarde?
Hoe beschrijven wetenschappers de aarde?  NASA-beelden wijzen op een verdwijnende Kalmaegi
NASA-beelden wijzen op een verdwijnende Kalmaegi Waarom vervalt El Niño sneller dan La Niña?
Waarom vervalt El Niño sneller dan La Niña? Welk geografisch kenmerk is gedefinieerd bevroren boomloze landschap?
Welk geografisch kenmerk is gedefinieerd bevroren boomloze landschap?  Hoe het mondiale klimaat de sedimentaanvoer en de watercondities van het bassin in een jonge kloof beïnvloedt
Hoe het mondiale klimaat de sedimentaanvoer en de watercondities van het bassin in een jonge kloof beïnvloedt
Hoofdlijnen
- Wanneer twee cellen met N -aantal chromosomen fuseren, welk type cel resulteren?
- Wat is het exosysteem?
- Prokaryoten met een staafvorm worden genoemd?
- Wat is het bijvoeglijk naamwoord voor organisme?
- Wat ontvangt eiwitten en andere nieuw gevormde materialen verdelen ze over delen van de cel?
- Wat groeit meer bacteriënbouillon of agar?
- Wat is de definitie van organisatie in de wetenschap?
- De suiker-fosfaatruggen van de DNA Double Helix zijn in tegengestelde richtingen georiënteerd?
- Wat wordt één gelijkenis gedeeld door osmose en vergemakkelijkte diffusie?
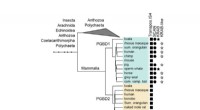
- Warmteminnende Australische mieren geloven in diversiteit, hint 74 soorten nieuw voor de wetenschap

- Hoe meten we pijn?

- Een nieuw gen bij zoogdieren dat een nieuwe structuur in zenuwcellen aanstuurt
- Citroenfruit versterken om beter bestand te zijn tegen klimaatverandering

- Microbieel moordmysterie opgelost
 Wat zijn decomponetten van het wetenschappelijke onderzoek?
Wat zijn decomponetten van het wetenschappelijke onderzoek?  Berichten op sociale media kunnen aangeven of een protest gewelddadig zal worden
Berichten op sociale media kunnen aangeven of een protest gewelddadig zal worden Wat is de Atshenosphere?
Wat is de Atshenosphere?  Kan het additieve boommodel machine learning in de geneeskunde uitbreiden?
Kan het additieve boommodel machine learning in de geneeskunde uitbreiden? Welke wetenschapper bestudeert gewassen en bodem?
Welke wetenschapper bestudeert gewassen en bodem?  Wie ontwikkelde Astrolabe?
Wie ontwikkelde Astrolabe?  Wat maakt een verbinding zuur en basisch?
Wat maakt een verbinding zuur en basisch?  Hoe noem je stoffen die worden gemaakt door een chemische reactie?
Hoe noem je stoffen die worden gemaakt door een chemische reactie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

