
Wetenschap
Gebruik van in adavosertib ingekapselde MOF's voor de behandeling van p53-gemuteerde galblaaskanker via synthetische letaliteit
Sinds de onthulling van poly(ADP-ribose) polymerase (PARP)-remmers en hun opmerkelijke resultaten bij de behandeling van BRCA1/2-mutante kankers, heeft synthetische letaliteit (SL) bij antitumortherapie steeds meer aandacht getrokken. SL is een fenomeen waarbij één enkele genetische gebeurtenis onvoldoende is om celdood te veroorzaken, maar meerdere genetische gebeurtenissen tot celdood leiden.
De karakterisering van genetische SL-interacties met tumorspecifieke mutaties kan worden gebruikt om een conceptueel raamwerk te ontwikkelen voor het aanpakken van "niet-ruggeerbare" doelen zoals het tumorsuppressorgen p53. Galblaaskanker (GBC) is de meest voorkomende kwaadaardige tumor van het galstelsel en is doorgaans fataal vanwege de beperkte werkzaamheid van de bestaande behandeling.
Er is gerapporteerd dat p53 een van de meest frequent gemuteerde genen is en een slechte prognostische marker bij GBC. Daarom is een op SL gebaseerde strategie voor het targeten van p53-gemuteerde GBC een veelbelovende aanpak.
Een nieuwe studie over dit onderwerp onder leiding van prof. Mingyu Chen, prof. Xiujun Cai, dr. Shjie Li, dr. Sarun Juengpanich en dr. Win Topatana, allen van het Sir Run-Run Shaw Hospital, Zhejiang University, en prof. Jicheng Yu van het College of Pharmaceutical Sciences, Zhejiang University verschijnt in Science Bulletin .
Eerdere studies hebben aangetoond dat herstel van DNA-schade dat door WEE1 wordt bereikt door de regulatie van het G2-controlepunt in de celcyclus essentieel is voor de overleving van p53-gemuteerde cellen. Daarom heeft adavosertib (ADA), een WEE1-remmer, een significant synthetisch dodelijk effect op p53-gemuteerde kankers. Geneesmiddelenresistentie als gevolg van compensatieroutes voor DNA-schade (DDR) en hoge toxiciteit beperken echter verdere toepassingen.
Recente onderzoeken hebben aangetoond dat het gebruik van fysieke factoren zoals fotodynamische therapie (PDT), sonodynamische therapie (SDT) en gastherapie bij de behandeling van tumoren superieure effecten en een breder scala aan toepassingen heeft dan conventionele chemische geneesmiddelen. Fysieke factoren zorgen voor onomkeerbare omstandigheden om het synthetische dodelijke effect van het doden van tumoren te versterken en zullen een effectieve strategie blijken te zijn.
Gebaseerd op het vermogen van de MOF-structuur om verschillende aanvullende omstandigheden te realiseren tijdens het afleveren van medicijnen, selecteerde deze nieuwe studie MOF als een hulpmiddel in combinatie met SDT om het synthetische dodelijke effect tussen WEE1 en p53 in GBC te versterken en behaalde een veelbelovend resultaat.
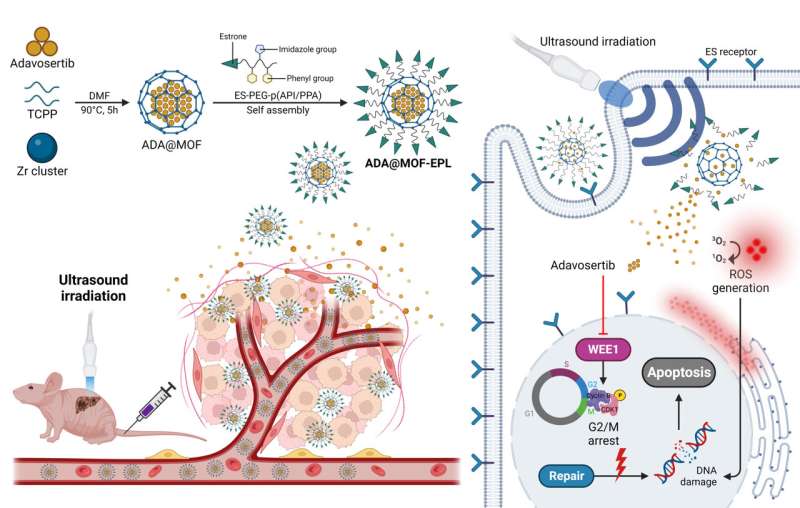
P>Specifiek werd een sonosensitieve porfyrine (tetrakis (4-carboxyfenyl) porfyrine, TCPP)-bevattende Zr-MOF gebruikt als de organische ruggengraat voor sonodynamische therapie (SDT), gevolgd door ADA-inkapseling tijdens de éénpots-MOF-synthese om de ADA-belasting te verhogen. van MOF's (ADA@MOF). Bovendien werd het oppervlak van ADA@MOF gecoat met pH-responsieve op oestron gerichte polymere liganden (EPL's) om de nanodeeltjes een tumorgericht vermogen te geven (ADA@MOF-EPL).
Vanwege de hoge expressie van de oestrogeenreceptor (ER) in GBC, functioneert oestron als een tumorgericht ligand, waardoor nanodeeltjes snel en nauwkeurig de celkern kunnen binnendringen en zich ophopen. Bij het binnendringen in de zure tumor-micro-omgeving (TME) zullen de verzwakte ionische interacties tussen ADA@MOF en EPL de structuur losmaken, wat leidt tot de initiële afgifte van ADA.
Vervolgens zal bestraling met ultrageluid (VS) om de sonosensitieve porfyrinebevattende MOF te stimuleren resulteren in de versnelde afgifte van ADA en ROS genereren voor beschadigend DNA. Dit zal een hogere gevoeligheid van p53-gemuteerde kankercellen voor ADA veroorzaken en resistentie tegen geneesmiddelen vermijden als gevolg van DDR-compensatieroutes aan de bron.
Het versterkte synthetische dodelijke effect tussen ADA en p53 door een aanvullende voorwaarde van SDT zou dus een robuust tumordodend vermogen hebben. Bovendien verminderen de nanodeeltjes ook de toxische reactie van het medicijn aanzienlijk. Het allerbelangrijkste is dat deze nieuwe studie een nieuw perspectief biedt op het gebruik van op MOF gebaseerde medicijnafgiftesystemen bij de behandeling van verschillende refractaire vormen van kanker via verbeterde SL.