
Wetenschap
Intermoleculaire krachten begrijpen:samengestelde sterkten vergelijken
1. Type IMF:
* Waterstofbinding: Het sterkste type IMF, gevormd tussen een waterstofatoom gebonden aan een zeer elektronegatief atoom (O, N of F) en een eenzaam elektronenpaar op een ander elektronegatief atoom.
* Dipool-dipoolinteracties: Komen voor tussen polaire moleculen vanwege de permanente dipolen die ze bezitten.
* London Dispersion Forces (LDF): Aanwezig in alle moleculen en voortkomend uit tijdelijke fluctuaties in de elektronenverdeling die tijdelijke dipolen creëren. De LDF-sterkte neemt toe met de moleculaire grootte en het oppervlak.
* Ion-dipoolinteracties: Komen voor tussen ionen en polaire moleculen.
2. Moleculaire structuur:
* Vorm: Lineaire moleculen hebben sterkere LDF dan vertakte moleculen vanwege een groter oppervlak.
* Polariteit: Polaire moleculen hebben sterkere IMF's dan niet-polaire moleculen vanwege dipool-dipoolinteracties.
* Grootte: Grotere moleculen hebben een sterkere LDF vanwege de grotere elektronenwolkgrootte en polariseerbaarheid.
3. Moleculair gewicht:
* Zwaardere moleculen hebben over het algemeen een sterkere LDF vanwege de grotere elektronenwolkgrootte.
Hier is een algemene richtlijn voor het vergelijken van IMF's:
* Waterstofbinding> Dipool-Dipool> London Dispersion Forces
Voorbeeld:
* Water (H2O) versus methaan (CH4): Water heeft waterstofbindingen vanwege de aanwezigheid van O-H-bindingen, terwijl methaan alleen LDF heeft. Daarom heeft water sterkere IMF's en een hoger kookpunt.
Volg deze stappen om de relatieve sterkte van IMF's in twee verbindingen effectief te vergelijken:
1. Identificeer het dominante IMF in elke verbinding.
2. Denk na over de moleculaire structuur en grootte van elke verbinding.
3. Vergelijk de kracht van de IMF's op basis van de hierboven genoemde factoren.
Onthoud:
* Sterkere IMF's leiden tot hogere smeltpunten, kookpunten en verdampingsenthalpie.
* Hoe polairder en groter een molecuul is, hoe sterker de IMF’s waarschijnlijk zullen zijn.
Door deze factoren te analyseren, kun je weloverwogen vergelijkingen maken over de relatieve sterkte van intermoleculaire krachten in verschillende verbindingen.
 Is N2 een vaste stof bij kamertemperatuur?
Is N2 een vaste stof bij kamertemperatuur?  Wat gebeurt er als je NaCl MgSO4 en H2O verwarmt?
Wat gebeurt er als je NaCl MgSO4 en H2O verwarmt?  Wat is de moleculaire vorm van PH3 CH4 HCLO N2 CH3NH2 H2CO C2H2 CH3CL HCOOH HCN H2O2?
Wat is de moleculaire vorm van PH3 CH4 HCLO N2 CH3NH2 H2CO C2H2 CH3CL HCOOH HCN H2O2?  Het identificeren van chemische reacties bij de verbranding van steenkool:bewijs en uitleg
Het identificeren van chemische reacties bij de verbranding van steenkool:bewijs en uitleg  Wat is dodelijke fase en hoe wordt het berekend?
Wat is dodelijke fase en hoe wordt het berekend?
Hoofdlijnen
- Waaruit bestaat de celwand van plantencellen?
- Welk type nucleïnezuur is de genetische materiaalcel?
- Waar is de eiercel van een plant gevestigd?
- Waar ontwikkelt het menselijke embryo zich?
- Parasieten onthullen hoe de evolutie een oude nucleaire structuur heeft gevormd
- Welk deel van de cel maakt eiwitten?
- Wat zijn organismen en wat maakt ze goed?
- Welke endocriene klieren zijn er in paren?
- Nieuwe ontdekking van een mechanisme dat de celdeling controleert
- Lensloos on-chip microscopieplatform toont dia's in volledig beeld

- Afbeelding:Prototype atoominterferometer

- Nieuw volledig glasvezelapparaat vereenvoudigt op vrije ruimte gebaseerde distributie van kwantumsleutels

- Onderzoekers bedenken nieuwe manier om licht te laten interageren met materie

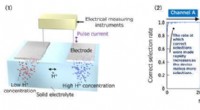
- Ionische beslisser in staat tot zelflerend
 Wat zijn enkele feiten over planeten?
Wat zijn enkele feiten over planeten?  Wat is de studie van ontwikkelingsorganismen van tijdsbestek tot hun uitkomen of geboorte?
Wat is de studie van ontwikkelingsorganismen van tijdsbestek tot hun uitkomen of geboorte?  Welke soorten sterren komen het meest voor in een nieuw gevormd sterrencluster?
Welke soorten sterren komen het meest voor in een nieuw gevormd sterrencluster?  Hoe verschijnt de maan tijdens een volle maan aan een waarnemer op aarde?
Hoe verschijnt de maan tijdens een volle maan aan een waarnemer op aarde?  De zon gaat onder op onhoudbare lange afstanden, toerisme voor kort verblijf, van regionale reisbubbels de toekomst maken
De zon gaat onder op onhoudbare lange afstanden, toerisme voor kort verblijf, van regionale reisbubbels de toekomst maken Cacaobonen zijn schaars:wat dit betekent voor boeren, bedrijven en chocoladeliefhebbers
Cacaobonen zijn schaars:wat dit betekent voor boeren, bedrijven en chocoladeliefhebbers  Waar ter wereld kun je vulkanen vinden?
Waar ter wereld kun je vulkanen vinden?  Hoe klimaatwetenschappers de mysteries van de Zuidelijke Oceaan ontrafelen
Hoe klimaatwetenschappers de mysteries van de Zuidelijke Oceaan ontrafelen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

