
Wetenschap
Wat gebeurt er met het licht van een bepaalde frequentie die atomen tegenkomt dezelfde resonantiefrequentie?
De basis:
* Resonantfrequentie: Elk atoom heeft specifieke frequenties waarbij het energie kan absorberen of uitzenden. Deze frequenties worden bepaald door de energieniveaus van de elektronen in het atoom.
* Licht als energie: Licht is een vorm van elektromagnetische straling die energie draagt in de vorm van fotonen. De energie van een foton is recht evenredig met de frequentie ervan.
Wat gebeurt er:
1. absorptie: Wanneer een foton van licht met dezelfde frequentie als de resonantiefrequentie van het atoom het atoom raakt, absorbeert het elektron in het atoom de energie van het foton. Hierdoor springt het elektron naar een hoger energieniveau.
2. opgewonden toestand: Het atoom is nu in een opgewonden staat. Het is onstabiel en wil terugkeren naar zijn grondtoestand (laagste energieniveau).
3. emissie: Het opgewonden atoom zal uiteindelijk de geabsorbeerde energie vrijgeven door een foton van licht uit te zenden met dezelfde frequentie als het geabsorbeerde foton. Dit uitgezonden licht kan in dezelfde richting zijn als het binnenkomende licht of in een andere richting.
Belangrijke gevolgen:
* transparantie: Als de lichtfrequentie aanzienlijk verschilt van de resonantiefrequentie van het atoom, gaat het licht door het materiaal (wees transparant).
* absorptie: Als de lichtfrequentie overeenkomt met de resonantiefrequentie van het atoom, wordt het licht geabsorbeerd, waardoor de intensiteit wordt verminderd. Dit is de reden waarom bepaalde materialen gekleurd lijken - ze absorberen specifieke golflengten van licht.
* emissie: Het uitgezonden licht kan worden gebruikt in verschillende toepassingen, zoals lasers en fluorescerende verlichting.
Voorbeeld:
Stel je een stemvork voor die trilt met een specifieke frequentie. Als u een andere tuningvork slaat met dezelfde frequentie in de buurt, begint deze ook te trillen. Dit is analoog aan resonerende absorptie in atomen.
Samenvattend:
Wanneer het licht van een specifieke frequentie atomen tegenkomt met dezelfde resonantiefrequentie, wordt het licht geabsorbeerd, waardoor de atomen opgewonden raken. Deze geëxciteerde atomen maken vervolgens het licht van dezelfde frequentie opnieuw en dragen bij aan fenomenen zoals transparantie, kleur en lichtemissie.
 Waarom filtert u blauwe kopersulfaatoplossing?
Waarom filtert u blauwe kopersulfaatoplossing?  Waarom wordt zwavel in chemische vergelijkingen geschreven als S en niet als S8?
Waarom wordt zwavel in chemische vergelijkingen geschreven als S en niet als S8?  Hoe weet u of een samengestelde neerslag na substitutiereactie?
Hoe weet u of een samengestelde neerslag na substitutiereactie?  Welke soorten atomen zou u verwachten in het element natrium te vinden?
Welke soorten atomen zou u verwachten in het element natrium te vinden?  Covalente koolstof-koolstofbindingen veel flexibeler dan verondersteld
Covalente koolstof-koolstofbindingen veel flexibeler dan verondersteld
Hoofdlijnen
- De voor- en nadelen van mutatie
- Wat zijn enkele voorbeelden van aanpassingsdieren en planten?
- Wetenschapsprojecten: een skelet maken
- De spieren van het menselijk lichaam onthouden
- Onderzoekers:We hielpen boeren net zo gemakkelijk toegang te krijgen tot toekomstige klimaatprojecties als het controleren van het weer
- Aangrenzende hartspiercellen zijn stevig bevestigd aan elkaars gemodificeerde plasmamembranen die worden genoemd?
- Archeologie en ecologie geven samen een vollediger beeld van vroegere relaties tussen mens en natuur
- Waarom is stikstof belangrijk voor planten?
- Wat zijn enkele goede DNA-wetenschapsprojecten?
- Onderzoekers suggereren wijziging van het kwantumversleutelingssysteem met compacte detector

- Astronomen gebruiken bellen om WIMP's te zoeken

- Skyrmions kan gegevensopslag van de volgende generatie bieden

- Een vacuüm ultraviolet foto-ionisatie time-of-flight massaspectrometer om de gasfase radicale reactie te analyseren
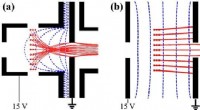
- Stroom die wordt gegenereerd wanneer licht een materiaal raakt, onthult elektronen die zich gedragen als een ongrijpbaar deeltje
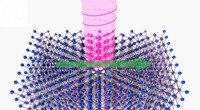
 Wat is het verschil tussen wet van natuurbeschermingsenergie en momentum?
Wat is het verschil tussen wet van natuurbeschermingsenergie en momentum?  Ingrediënten in Fingerprinting Powder
Ingrediënten in Fingerprinting Powder  Wat is het verband tussen getijden en maanfasen?
Wat is het verband tussen getijden en maanfasen?  Wat zijn de 6 belangrijkste kristallijne structuren van silicaatmineralen?
Wat zijn de 6 belangrijkste kristallijne structuren van silicaatmineralen?  Eerste toepassing van de eye-tracking-methodologie bij het bestuderen van de lithische industrie
Eerste toepassing van de eye-tracking-methodologie bij het bestuderen van de lithische industrie "Identification of Wasps
"Identification of Wasps Welk golftype heeft een frequentie van 23808 GHz?
Welk golftype heeft een frequentie van 23808 GHz?  Pleiades
Pleiades
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

