
Wetenschap
Wat is de gemiddelde snelheid van atomen in 2,00 mol neon bij 308 K?
1. Begrijp het concept
De gemiddelde snelheid van gasdeeltjes is gerelateerd aan hun kinetische energie, die recht evenredig is met de temperatuur. We kunnen de root-mean-square (RMS) snelheid gebruiken om deze gemiddelde snelheid weer te geven.
2. Formule
De RMS -snelheid (V rms ) wordt gegeven door:
v rms =√ (3RT/M)
waar:
* R is de ideale gasconstante (8.314 J/mol · k)
* T is de temperatuur in Kelvin
* M is de molaire massa van het gas in kg/mol
3. Bereken de molaire massa van neon
Neon heeft een atoommassa van ongeveer 20,18 g/mol. Converteer dit naar kg/mol:
M =20,18 g/mol * (1 kg/1000 g) =0,02018 kg/mol
4. Sluit de waarden aan aan
v rms =√ (3 * 8.314 j/mol · k * 308 k/0.02018 kg/mol)
5. Bereken het resultaat
v rms ≈ 517 m/s
Daarom is de gemiddelde snelheid van neonatomen in 2,00 mol neon bij 308 K ongeveer 517 m/s.
Belangrijke opmerking: Het aantal mol (2,00 mol) heeft geen invloed op de gemiddelde snelheid. De RMS -snelheid hangt alleen af van de temperatuur en de molaire massa van het gas.
 In welke laag van de atmosfeer komt dit molecuul het meest voor?
In welke laag van de atmosfeer komt dit molecuul het meest voor?  Malaria kan worden geveld door een Antarctische zeespons
Malaria kan worden geveld door een Antarctische zeespons Wat zijn elementen die diatomaire moleculen vormen die gewoonlijk aan deze kant van het periodiek systeem worden gevonden?
Wat zijn elementen die diatomaire moleculen vormen die gewoonlijk aan deze kant van het periodiek systeem worden gevonden?  Wat is het percentage samenstelling van gassen die de atmosfeer vormen?
Wat is het percentage samenstelling van gassen die de atmosfeer vormen?  Wat zijn de verschillen tussen metalen en niet -metalen?
Wat zijn de verschillen tussen metalen en niet -metalen?
 Koudste temperatuur op het noordelijk halfrond officieel bevestigd
Koudste temperatuur op het noordelijk halfrond officieel bevestigd Wat is een voorbeeld van interspecifieke concurrentie in het naaldbos?
Wat is een voorbeeld van interspecifieke concurrentie in het naaldbos?  Degraderende permafrost brengt de Arctische infrastructuur tegen het midden van de eeuw in gevaar
Degraderende permafrost brengt de Arctische infrastructuur tegen het midden van de eeuw in gevaar Onderzoekers verbeteren internationale nomenclatuur van aardverschuivingsgeometrie
Onderzoekers verbeteren internationale nomenclatuur van aardverschuivingsgeometrie Nieuw onderzoek legt uit hoe inheemse bomen hittegolven uitzweten
Nieuw onderzoek legt uit hoe inheemse bomen hittegolven uitzweten
Hoofdlijnen
- Wat is de vorm van een levercel voor dieren en waarom?
- Welke organismen vormen een fossiel?
- Wat eenzame slakken ons kunnen vertellen over de effecten van stress op het geheugen
- Wat zijn 2 overeenkomsten en verschillen van een plantendiercel?
- Nieuwe formule voorspelt hoe mensen de komende decennia zullen migreren
- Beschrijf de verschillende kenmerken van het leven?
- Hoe heet het zaaddragende orgaan van een bloem?
- Welke vertakkingsstructuren dragen informatie naar het cellichaam van een neuron?
- Begrijpen hoe een cel een persoon wordt, met wiskunde
- Onderzoekers boeken vooruitgang bij het commercialiseren van vereenvoudigde dual-comb spectroscopie

- Bananenspots kunnen voedselverspilling tegengaan, blijkt uit onderzoek

- Een topologische vingerafdruk identificeren
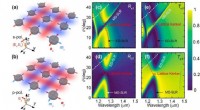
- Dual-lattice Kerker-effecten:lichtverstrooiing regelen met invallende polarisatie en hoek
- Een revolutionaire methode om strooilicht op ruimtetelescopen drastisch te verminderen

 Welke heeft het grootste effect zon of maan?
Welke heeft het grootste effect zon of maan?  Welke eilanden bevinden zich op het puntje van Schotland?
Welke eilanden bevinden zich op het puntje van Schotland?  ATLAS Experiment bestudeert de dynamiek van top-quarks met een zeer hoog momentum
ATLAS Experiment bestudeert de dynamiek van top-quarks met een zeer hoog momentum Onderzoekers optimaliseren materiaalontwerp met behulp van computationele technologieën
Onderzoekers optimaliseren materiaalontwerp met behulp van computationele technologieën Laat de spermaraces beginnen
Laat de spermaraces beginnen Waar zijn fossiele brandstoffen voor?
Waar zijn fossiele brandstoffen voor?  Zenden alle zenders een continue golf of een gepulseerde golfvorm uit?
Zenden alle zenders een continue golf of een gepulseerde golfvorm uit?  ALMA vindt ingrediënt van leven rond baby-zonachtige sterren
ALMA vindt ingrediënt van leven rond baby-zonachtige sterren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

