
Wetenschap
Welke verbindingen worden gevormd wanneer ijzer en zink reageren?
Dit is waarom:
* reactiviteitsreeks: IJzer is reactiever dan zink. Dit betekent dat ijzer zink zou verplaatsen van zijn verbindingen, niet andersom. Deze verplaatsingsreactie treedt echter alleen voor in aanwezigheid van een oplossing die zinkionen bevat (zoals zinksulfaat).
* Geen directe reactie: In hun elementaire vormen zullen ijzer en zink niet reageren om nieuwe verbindingen te vormen.
Om een reactie te observeren, zou u moeten:
* Introduceer een verbinding die zinkionen bevat: Als u bijvoorbeeld ijzer in een oplossing van zinksulfaat (ZnSo₄) plaatst, zou het ijzer het zink verplaatsen, ijzersulfaat (FESO₄) vormen en zink als een vaste stof achterlaten.
* Gebruik een elektrochemische cel: Je zou een elektrochemische cel kunnen maken waar ijzer werkt als de anode en zink werken als de kathode. Dit zou een redoxreactie mogelijk maken, maar geen directe reactie tussen de twee metalen.
Laat het me weten als je nog andere vragen hebt!
 Welke chemische eigenschap zorgt ervoor dat er roest ontstaat op een spijker?
Welke chemische eigenschap zorgt ervoor dat er roest ontstaat op een spijker?  Hoeveel atomen vormen 1 molecuul ammoniak?
Hoeveel atomen vormen 1 molecuul ammoniak?  Wat is de dichtheid van zwaveldioxidegas SO2 bij 475 mm Hg en 58,5 ° C?
Wat is de dichtheid van zwaveldioxidegas SO2 bij 475 mm Hg en 58,5 ° C?  Nieuwe katalysator verhoogt radicaal de omzettingssnelheid van koolstofdioxide in zonnebrandstoffen
Nieuwe katalysator verhoogt radicaal de omzettingssnelheid van koolstofdioxide in zonnebrandstoffen Wetenschappers analyseren de chemische bindingen die eiwitten vormen
Wetenschappers analyseren de chemische bindingen die eiwitten vormen
Hoofdlijnen
- Hoe overleven blinde grotvissen hun zuurstofarme omgeving?
- Hoe noem je de wetenschappelijke studie van metingen dat het menselijk lichaam heeft gebruikt als een vorm forensische wetenschap?
- Hoe is de taal geëvolueerd?
- Wetenschappers vragen zich af:hoe kunnen vloeibare organellen in cellen naast elkaar bestaan zonder te fuseren?
- Wat zijn de drie soorten modellen die door wetenschappers worden gebruikt?
- Grootte doet er niet toe - althans voor hamerhaaien en zwemprestaties
- Wie geeft je meer DNA je moeder of vader?
- Organismen die lichtenergie van de zon opvangen en in voedsel omzetten, worden?
- Is sommige microorgamisme beter bestand tegen hitte dan anderen?
- Hoogwaardige katalysatoren met één atoom voor brandstofcellen bij hoge temperaturen

- Eco-lijm kan schadelijke lijmen in houtconstructies vervangen

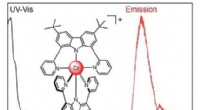
- Een nieuw chroomcomplex zendt licht uit in de ongrijpbare NIR-II-golflengte
- Tweefasig materiaal met verrassende eigenschappen

- Mobiel apparaat kan het gemakkelijker maken om schadelijke algenbloei te voorspellen en te beheersen

 Wat is de chemische formule voor waterstof en fosfaat?
Wat is de chemische formule voor waterstof en fosfaat?  Wat is het klimiet in tropen en Noordpoolgebied?
Wat is het klimiet in tropen en Noordpoolgebied?  Wat is de naam van een georganiseerde groepscellen die samenwerken?
Wat is de naam van een georganiseerde groepscellen die samenwerken?  Welke temperatuur heeft dezelfde numerieke waarde in Kelvin en Celsius?
Welke temperatuur heeft dezelfde numerieke waarde in Kelvin en Celsius?  Wanneer 430 J werk wordt gedaan op een systeem, verloor het 120 energie als warmte de waarde van de waarde berekent voor dit proces?
Wanneer 430 J werk wordt gedaan op een systeem, verloor het 120 energie als warmte de waarde van de waarde berekent voor dit proces?  Wat zijn enkele interessante vragen over sterrenstelsels die wetenschappers momenteel onderzoeken?
Wat zijn enkele interessante vragen over sterrenstelsels die wetenschappers momenteel onderzoeken?  Hoeveel mensen morgen? De Verenigde Naties herzien hun prognoses
Hoeveel mensen morgen? De Verenigde Naties herzien hun prognoses Waarom wilde Apollo Cassandra?
Waarom wilde Apollo Cassandra?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

