
Wetenschap
Waterstofperoxide versus benzoylperoxide:belangrijkste verschillen en toepassingen
Door Vincent Zomers
Bijgewerkt op 24 maart 2022
Burke/Triolo Productions/Brand X Pictures/Getty Images
Chemische verbindingen met vergelijkbare formules vertonen vaak verschillende eigenschappen en toepassingen. Een bekend voorbeeld is het contrast tussen waterstofcyanide (HCN) en methylcyanide (MeCN), waarbij de eerste een dodelijk gif is en de laatste vooral als oplosmiddel dient. Op dezelfde manier delen waterstofperoxide (H₂O₂) en benzoylperoxide een vergelijkbare peroxide-ruggengraat, maar ze lopen aanzienlijk uiteen in hun gedrag en gebruik.
Chemische structuur
De formule van waterstofperoxide, H₂O₂, weerspiegelt water (H₂O) met een extra zuurstofatoom, waardoor het unieke oxiderende eigenschappen heeft. Benzoylperoxide daarentegen bevat een fenylring (Ph‑) en wordt gewoonlijk weergegeven als (Ph‑CO)₂O₂.
Reactiviteit
Bij verhitting of katalyse valt waterstofperoxide uiteen in water en zuurstof:
2 H₂O₂ → 2 H₂O + O₂
Benzoylperoxide reageert daarentegen met water en levert benzoëzuur en zuurstof op:
2 (PhCO)₂O₂ + 2 H₂O → 4 PhCOOH + 3 O₂
In tegenstelling tot waterstofperoxide is benzoylperoxide slecht oplosbaar in water en heeft het de neiging een film te vormen bij het aanbrengen. Warmte kan benzoylperoxide ook in twee benzoyloxyradicalen splitsen:
(PhCO)₂O₂ + heat → 2 PhCOO·
Deze generatie radicalen ligt ten grondslag aan het wijdverbreide gebruik ervan als initiator van vrije radicalen bij polymerisatie en andere organische syntheses.
Praktische toepassingen
Waterstofperoxide heeft de voorkeur in omgevingen waar filmvorming ongewenst is. De sterke oxiderende kracht maakt het ideaal voor het bleken van haar, het desinfecteren van kleine wonden en het dienen als bleekmiddel bij de papierproductie.
De neiging van benzoylperoxide om een film te vormen en vrije radicalen te genereren, maakt het geschikt voor cosmetisch gebruik zoals het bleken van tanden en de behandeling van acne. Het vermogen om polymerisatie te initiëren positioneert het ook als een cruciaal reagens bij de industriële polymeerproductie en verschillende organische transformaties.
 Welke van de volgende is een organisch molecuul?
Welke van de volgende is een organisch molecuul?  Keramische honingraatluchtfilters kunnen stadsvervuiling verminderen
Keramische honingraatluchtfilters kunnen stadsvervuiling verminderen Waterstofperoxide-experimenten
Waterstofperoxide-experimenten  Elektrolytboost verbetert de prestaties van waterige dual-ion-batterijen
Elektrolytboost verbetert de prestaties van waterige dual-ion-batterijen Onderzoekers vinden nieuwe techniek voor het afstemmen van de kleur van LED-lichtemissie
Onderzoekers vinden nieuwe techniek voor het afstemmen van de kleur van LED-lichtemissie
Hoofdlijnen
- Wat is de structuur van bloed?
- Wat zijn de velden van biotechnologie?
- Wat is de moleculaire formule voor bèta-globin?
- Hoe DNA en een supercomputer kunnen helpen de honingbijpopulaties in stand te houden
- Wat is de chemische samenstelling van een cel?
- Wat zijn het verschil dat wetenschap wordt geprojecteerd?
- Wat zijn twee functies van het uitscheidingssysteem?
- Hoe maakt de Calvin -cyclus suiker?
- Wat is een voorbeeld van een meercellige schimmels?
- Veenbessen kunnen darmgezondheidsproblemen voor vleeseters verminderen

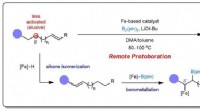
- Duurzame ijzerkatalyse maakt controleerbare alkeenborylering mogelijk
- Lasertechnieken en fotochemie vinden ongrijpbare moleculaire bouwsteen
- Het verminderen van zout in Parmigiano Reggiano-kaas heeft mogelijk geen negatieve invloed op de smaak

- Wetenschappers ontwikkelen vulmiddelskelet met ijsmatrijs met verbeterde thermische geleidbaarheid

 Hoe reist de zenuwimpuls langs een axon?
Hoe reist de zenuwimpuls langs een axon?  Niet alleen brood en bier:microben kunnen koolstofdioxide fermenteren om ook brandstof te maken
Niet alleen brood en bier:microben kunnen koolstofdioxide fermenteren om ook brandstof te maken In het konijnenhol:hoe elektronen door exotisch nieuw materiaal reizen
In het konijnenhol:hoe elektronen door exotisch nieuw materiaal reizen  Uiterst nauwkeurige metingen van atoomtoestanden voor kwantumcomputers
Uiterst nauwkeurige metingen van atoomtoestanden voor kwantumcomputers Wanneer ontploft uw zon?
Wanneer ontploft uw zon?  Welk organisme scheiden ureum uit?
Welk organisme scheiden ureum uit?  Onderzoek werpt nieuw licht op hoe bodemvirussen zich gedragen en interageren met bacteriën
Onderzoek werpt nieuw licht op hoe bodemvirussen zich gedragen en interageren met bacteriën  Waarom werd verwarmde gassen lichter?
Waarom werd verwarmde gassen lichter?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

