
Wetenschap
Energieniveaus in het periodiek systeem uitgelegd
Door Corina Fiore Bijgewerkt op 24 maart 2022
BananaStock/BananaStock/Getty Images
Het periodiek systeem is georganiseerd in kolommen en rijen. Het aantal protonen in de kern neemt toe bij het lezen van het periodiek systeem van rechts naar links. Elke rij vertegenwoordigt een energieniveau. De elementen in elke kolom delen vergelijkbare eigenschappen en hetzelfde aantal valentie-elektronen. Valentie-elektronen zijn het aantal elektronen in het buitenste energieniveau.
Aantal elektronen
Tomasz Wyszoamirski/iStock/Getty Images
Aantal elektronen
Het aantal elektronen in elk energieniveau wordt weergegeven in het periodiek systeem. Het aantal elementen in elke rij laat zien hoeveel elektronen er nodig zijn om elk niveau te vullen. Waterstof en helium staan in de eerste rij of periode van het periodiek systeem. Daarom kan het eerste energieniveau in totaal twee elektronen bevatten. Het tweede energieniveau kan acht elektronen bevatten. Het derde energieniveau kan in totaal 18 elektronen bevatten. Het vierde energieniveau kan 32 elektronen bevatten. Volgens het Aufbau-principe zullen elektronen eerst de laagste energieniveaus vullen en pas in de hogere niveaus inbouwen als het energieniveau daarvoor vol is.
Orbitalen
Roman Sigaev/iStock/Getty Images
Orbitalen
Elk energieniveau bestaat uit gebieden die bekend staan als een orbitaal. Een orbitaal is een waarschijnlijkheidsgebied waarin elektronen kunnen worden gevonden. Elk energieniveau, behalve het eerste, heeft meer dan één orbitaal. Elke orbitaal heeft een specifieke vorm. Deze vorm wordt bepaald door de energie die de elektronen in de orbitaal bezitten. Elektronen kunnen willekeurig overal binnen de vorm van de orbitaal bewegen. De kenmerken van elk element worden bepaald door de elektronen in de orbitaal.
De S-orbitaal
Archeophoto/iStock/Getty Images
De S-orbitaal
De s-orbitaal heeft de vorm van een bol. De s-orbitaal is altijd de eerste die op elk energieniveau wordt ingevuld. De eerste twee kolommen van het periodiek systeem staan bekend als het s-blok. Dit betekent dat de valentie-elektronen voor deze twee kolommen in een s-orbitaal voorkomen. Het eerste energieniveau bevat alleen een s-orbitaal. Waterstof heeft bijvoorbeeld één elektron in de s-orbitaal. Helium heeft twee elektronen in de s-orbitaal, die het energieniveau vullen. Omdat het energieniveau van helium gevuld is met twee elektronen, is het atoom stabiel en reageert het niet.
De P-orbitaal
carloscastilla/iStock/Getty Images
De P-orbitaal
De p-orbitaal begint zich te vullen zodra de s-orbitaal op elk energieniveau is gevuld. Er zijn drie p-orbitalen per energieniveau, elk in de vorm van een propellerblad. Elk van de p-orbitalen bevat twee elektronen, zodat er in totaal zes elektronen in de p-orbitalen zitten. Volgens de regel van Hund moet elke p-orbitaal per energieniveau één elektron ontvangen voordat hij een tweede elektron verdient. Het p-blok begint met de kolom met boor en eindigt met de kolom met edelgassen.
De D- en F-orbitalen
agsandrew/iStock/Getty Images
De D- en F-orbitalen
De d- en f-orbitalen zijn zeer complex. Er zijn vijf d-orbitalen per energieniveau, te beginnen met het derde energieniveau. De overgangsmetalen vormen de d-orbitalen. Er zijn zeven f-orbitalen per energieniveau, te beginnen met het vijfde energieniveau. De lanthanide en actinide vormen de f-orbitalen.
Hoofdlijnen
- Wat zijn allemaal organismen in staat?
- Leg uit waarom osmose belangrijk is voor cellen?
- Definitie van de productregel in genetica?
- Wat draagt de informatie om een proteoom te produceren?
- Een natuurbehoudsraadsel:wanneer rattencontrole om de ene soort te behouden een andere soort bedreigt
- Welk deel van de vertaling hangt af van dezelfde basis paring -regel die wordt gebruikt bij transcriptie en DNA -replicatie?
- Wat is de staat van vrij zijn van alle pathogene micro -organismen?
- Hebben eukaryoten cellen enkele celorganismen?
- Beweging van organellen in het cytoplasma Planten- en diercellen is het meest direct te danken?
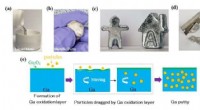
- Putty-achtige composieten van galliummetaal met potentieel voor toepassing in de echte wereld
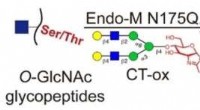
- Reversibele chemo-enzymatische labelstrategie maakt diepgaande analyse van eiwit O-GlcNAcylation mogelijk
- Een technologie om 2D-vlakken om te zetten in zachte en flexibele 3D-structuren door hechting tussen dunne films te ontwikkelen

- Onderzoek naar de deeltjesgrootte en depositie van dampen

- Legerwetenschappers ontdekken kracht in urine

 Wat is de ballistische constante?
Wat is de ballistische constante?  Roltrapetiquette:moet ik staan of lopen voor een efficiënte rit?
Roltrapetiquette:moet ik staan of lopen voor een efficiënte rit? Welke vergelijking wordt gebruikt om lichtsnelheid door materiaal te bepalen?
Welke vergelijking wordt gebruikt om lichtsnelheid door materiaal te bepalen?  Wat is Astrobelt?
Wat is Astrobelt?  Hoeveel suikergram in een kwart kopje suiker?
Hoeveel suikergram in een kwart kopje suiker?  Beschrijf wat er gebeurt met sediment als het wordt veranderd Sedimentair Rock?
Beschrijf wat er gebeurt met sediment als het wordt veranderd Sedimentair Rock?  Waar is het platste oppervlak ter wereld?
Waar is het platste oppervlak ter wereld?  Wat voor soort bacteriën was Anabaena?
Wat voor soort bacteriën was Anabaena?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


