
Wetenschap
Waarom transitiemetalen uitstekende katalysatoren zijn
Jason Reed/Photodisc/Getty Images
Overgangsmetalen – elementen zoals chroom, ijzer en nikkel – beschikken over valentie-elektronen in twee schillen, waardoor ze unieke katalytische eigenschappen krijgen. Omdat ze gemakkelijk elektronen kunnen doneren en accepteren, verlagen ze de reactiebarrières zonder de thermodynamica te veranderen.
Hoe katalysatoren werken
Katalysatoren versnellen reacties door een overgangstoestand met lagere energie te bieden, waardoor de frequentie van effectieve botsingen toeneemt terwijl de identiteit van de reactanten onveranderd blijft. Ze veranderen het algemene thermodynamische evenwicht niet.
Wat maakt een transitiemetaal
Hoewel alle overgangsmetalen tot het d-blok behoren, komt niet elk d-blokelement in aanmerking. Een echt overgangsmetaal bezit een onvolledig gevulde d-orbitaal, zoals scandium (Sc³⁺) of zink (Zn²⁺), die geen d-elektronen hebben en dus geen katalytisch gedrag vertonen.
Belangrijke katalytische eigenschappen van transitiemetalen
Hun vermogen om te schakelen tussen meerdere oxidatietoestanden en stabiele complexen te vormen, stelt hen in staat efficiënt elektronen uit te wisselen met substraten. Deze veelzijdigheid is de hoeksteen van hun katalytische prestaties.
Elektronendonor- en acceptormogelijkheden
Neem koper als voorbeeld:het komt van nature voor als Cu⁺, Cu²⁺ en Cu³⁺. Dankzij de gedeeltelijk gevulde d-orbitalen kan het fungeren als elektronendonor of -acceptor, waardoor redoxprocessen worden vergemakkelijkt die essentieel zijn voor veel katalytische cycli.
Mechanistische rol bij reacties
Overgangsmetalen coördineren met reactanten om metaalcomplexen te creëren. Als de overgangstoestand extra elektronen vereist, ondergaat het metaal oxidatie of reductie om deze te leveren. Omgekeerd kan het overtollige elektronendichtheid opslaan, tussenproducten stabiliseren en het reactiepad sturen.
Oppervlakte-interactiefactoren
Adsorptie- en absorptie-eigenschappen van zowel het metaal als zijn complexen beïnvloeden de katalytische efficiëntie verder, waardoor de manier wordt beïnvloed waarop substraten de actieve plaats benaderen en eraan binden.
 Wat is verstoorde regen en hoe het is gevormd?
Wat is verstoorde regen en hoe het is gevormd?  Wat is een reagens om aan te tonen dat een oxide -amfoterisch?
Wat is een reagens om aan te tonen dat een oxide -amfoterisch?  Hoe is een bruine kluizenaarspin als een samoeraienzwaardsmid?
Hoe is een bruine kluizenaarspin als een samoeraienzwaardsmid? Wat zijn enkele kenmerken van geleiding?
Wat zijn enkele kenmerken van geleiding?  Wat onderscheidt een verbinding zoals kopersulfaat van een gewoon mengsel van poederzwavel?
Wat onderscheidt een verbinding zoals kopersulfaat van een gewoon mengsel van poederzwavel?
 De verschillende soorten dieren en planten op Ben Nevis?
De verschillende soorten dieren en planten op Ben Nevis?  NASA volgt potentiële tropische cycloon 9 naar het oosten van de Caraïben
NASA volgt potentiële tropische cycloon 9 naar het oosten van de Caraïben Riolering en dierlijk afval met ernstige gevolgen voor de Britse kust, nieuw onderzoek concludeert
Riolering en dierlijk afval met ernstige gevolgen voor de Britse kust, nieuw onderzoek concludeert Hoe het meten van emissies in realtime steden kan helpen om netto nul te bereiken
Hoe het meten van emissies in realtime steden kan helpen om netto nul te bereiken Definitie van Vertical Climate
Definitie van Vertical Climate
Hoofdlijnen
- Waar worden Bohm -organen gemaakt?
- Wat zijn twee kenmerken die plantencellen hebben die dieren niet hebben?
- Kop of staart? Wetenschappers identificeren een gen dat de polariteit reguleert bij het regenereren van platwormen
- Universiteiten houden van interdisciplinaire STEM-programma’s, maar hoe zit het met studenten?
- Hoe verschillen bryophytes van andere plantendivisies?
- Welke niet -lymfocytencel is een centrale acteur in klonale selectie?
- Hoe een spanningssensor een integrale rol speelt bij de uitgelijnde chromosoompartitie
- Wat gebruikt reverse transcriptase van DNA?
- Vissenseks zo luid dat dolfijnen doof kunnen worden
- Door de spiegel:nieuwe spiegelbeeldmoleculen kunnen leiden tot betere medicijnen
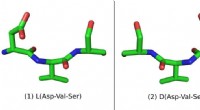
- Noodzaak van rigoureuze procedures binnen de elektrochemische productie van ammoniak

- Nieuw oplosmiddel draagt bij aan de volgende generatie biobrandstofproductie uit biomassa
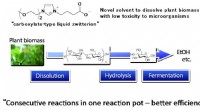
- Wetenschappers verkrijgen carbide met hoge entropie in elektrisch boogplasma

- Nieuwe modellen om de microstructuur van polymeermengsels te onderzoeken

 Is de binnenkant ballon vaste vloeistof of een gas?
Is de binnenkant ballon vaste vloeistof of een gas?  Planten kunnen de uitdagingen van de klimaatverandering weerstaan en herstellen van droogte door de chemische code van lignine aan te passen
Planten kunnen de uitdagingen van de klimaatverandering weerstaan en herstellen van droogte door de chemische code van lignine aan te passen Wanneer twee of meer atomen verbinden en elektronen delen, vormen ze een?
Wanneer twee of meer atomen verbinden en elektronen delen, vormen ze een?  Wat is de relevantie van de fysica voor de apotheek?
Wat is de relevantie van de fysica voor de apotheek?  Magnetite Vs. Meteorite
Magnetite Vs. Meteorite Curiosity Marsrover verkent een veranderend landschap
Curiosity Marsrover verkent een veranderend landschap De lengte van een sterren leven wordt bepaald door wat?
De lengte van een sterren leven wordt bepaald door wat?  Koelen met de koudste materie ter wereld
Koelen met de koudste materie ter wereld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

