
Wetenschap
Hoe de relatieve massa van atomen en moleculen te berekenen
Hoe je de relatieve massa van atomen en moleculen kunt berekenen
Relatieve massa is een hoeksteen van de moderne scheikunde, waardoor scheikundigen de massa van een atoom of molecuul kunnen uitdrukken ten opzichte van een universele standaard:een twaalfde van een koolstof-12-atoom. Omdat protonen en neutronen grofweg 1×10⁻²⁷kg wegen en elektronen 1×10⁻³⁰kg, maakt het gebruik van een eenvoudige, eenheidloze schaal berekeningen zowel intuïtief als nauwkeurig.
Wat is relatieve massa?
In dit systeem telt elk proton of neutron als 1 eenheid. Elektronen, die veel lichter zijn, worden uit de berekening weggelaten. De relatieve atomaire massa van een element is dus eenvoudigweg de som van zijn protonen en neutronen:
Relatieve atomaire massa =aantal protonen + aantal neutronen
Een waterstofatoom (1 proton, 0 neutronen) heeft bijvoorbeeld een relatieve massa van 1, terwijl een koolstof-12-atoom (6 protonen, 6 neutronen) een relatieve massa van 12 heeft.
De relatieve massa van een element bepalen
Periodieke tabellen vermelden voor elk element één enkele waarde, vaak een niet-geheel getal, omdat de meeste elementen bestaan als een mengsel van isotopen. De tabelwaarde is een gewogen gemiddelde op basis van de natuurlijke overvloed:
Gewogen gemiddelde =Σ (isotoopmassa × overvloed) / 100
Voor chloor is de berekening:
((35×75) + (37×25)) / 100 =35,5
De relatieve atoommassa die voor chloor wordt weergegeven, is dus 35,5.
Relatieve atomaire massa van specifieke isotopen
Wanneer er naar een bepaalde isotoop wordt verwezen, zoals uranium-238 —het getal na de elementnaam is de exacte relatieve massa (238). Als je de isotoop kent, kun je de massa rechtstreeks berekenen door protonen en neutronen toe te voegen.
Relatieve moleculaire massa berekenen
Zodra de relatieve atoommassa's bekend zijn, is de relatieve molecuulmassa van een verbinding de som van de bijdrage van elk element:
Relatieve molecuulmassa =Σ (aantal atomen van het element × relatieve atoommassa van dat element)
Voorbeelden:
- Water (H₂O) → (2×1) + (1×16) =18
- Zwavelzuur (H₂SO₄) → (2×1) + (1×32) + (4×16) =98
Pas dezelfde procedure toe op elke chemische formule.
Praktische tips
- Gebruik het lagere getal op het periodiek systeem voor snelle referentie, tenzij een specifieke isotoop vereist is.
- Onthoud dat de waarden eenheidloos zijn; ze vertegenwoordigen veelvouden van de koolstof-12-standaard.
- Voor complexe moleculen kan het opdelen van de formule in groepen (bijvoorbeeld CH₂, OH) de berekeningen vereenvoudigen.
Met deze principes kun je vol vertrouwen de relatieve massa van elk atoom of molecuul bepalen, of het nu gaat om academisch onderzoek of alledaagse scheikundige taken.
 Kan de handel in waterkwaliteit de vervuiling effectief verminderen?
Kan de handel in waterkwaliteit de vervuiling effectief verminderen?  Wetenschappers testen met succes nieuwe, veiligere titaniumplaat voor herstel van botweefsel
Wetenschappers testen met succes nieuwe, veiligere titaniumplaat voor herstel van botweefsel Fysica van ladingstransport van een unieke klasse van geconjugeerde polymeren met stijve staven
Fysica van ladingstransport van een unieke klasse van geconjugeerde polymeren met stijve staven Als het mengsel van elektrisch neutraal hoeveel meer bèta -deeltjes dan alfa in ballon zijn?
Als het mengsel van elektrisch neutraal hoeveel meer bèta -deeltjes dan alfa in ballon zijn?  Waar bevinden de lanthaniden zich op het periodieke tabel?
Waar bevinden de lanthaniden zich op het periodieke tabel?
 Nieuwe studie toont impact van grootschalige boomsterfte op koolstofopslag
Nieuwe studie toont impact van grootschalige boomsterfte op koolstofopslag Luchtcirculatie beïnvloedt vorst meer dan opwarming van de aarde - voorlopig
Luchtcirculatie beïnvloedt vorst meer dan opwarming van de aarde - voorlopig Houd het in de grond:wat we kunnen leren van campagnes tegen fossiele brandstoffen
Houd het in de grond:wat we kunnen leren van campagnes tegen fossiele brandstoffen Bomen in dit biome werpen hun bladeren af. De herfsttemperatuur varieert met seizoenen is de?
Bomen in dit biome werpen hun bladeren af. De herfsttemperatuur varieert met seizoenen is de?  Welke soorten planten leven in het aquatische bioma?
Welke soorten planten leven in het aquatische bioma?
Hoofdlijnen
- Hoe heeft de uitvinding van de microscoop de celtheorie beïnvloed?
- Wie heeft de studies uitgevoerd die basis vormden voor moderne genetica?
- Polyploïdie:hoe extra chromosomensets de overleving en het broedsucces verbeteren
- Welk organisme heeft gespecialiseerde organen voor de uitscheiding van mebolisch afval?
- Kavachi:de actieve onderwatervulkaan die veerkrachtige haaien herbergt
- Wat zijn de verschillen tussen traditionele biotechnologie en moderne biotechnologie?
- Bacteriën groeien het beste bij welke pH?
- Gedeelde kenmerken van eukaryotische en prokaryotische cellen
- Een rol of baan in zijn omgeving staat bekend als?
- Een methode om kristallen te construeren met een grote fractie reactieve facetten

- Nieuwe kooien om moleculen te vangen, verleggen de grenzen van het eiwitontwerp
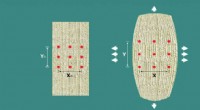
- 2D-materialen bieden unieke rekeigenschappen
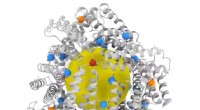
- Zinktransporter sleutel tot het bestrijden van alvleesklierkanker en meer

- Nieuw waargenomen eenwaardige calciumionen vertonen onverwachte metaalachtigheid en ferromagnetisme
 Hoe Amazon Echo luistert en wat het opslaat
Hoe Amazon Echo luistert en wat het opslaat  Een beter begrip van nanomaterialen
Een beter begrip van nanomaterialen Wat is de formule van loodsulfide?
Wat is de formule van loodsulfide?  Lavabuizen op Mars en de maan zijn zo breed dat ze planetaire bases kunnen herbergen
Lavabuizen op Mars en de maan zijn zo breed dat ze planetaire bases kunnen herbergen Onderzoekers ontwikkelen een genetische aanpak voor plantenregeneratie zonder de toepassing van fytohormonen
Onderzoekers ontwikkelen een genetische aanpak voor plantenregeneratie zonder de toepassing van fytohormonen  Wat voor soort planten groeien in Jamaica?
Wat voor soort planten groeien in Jamaica?  Wat zijn enkele landvormen gemaakt door chemische verwering?
Wat zijn enkele landvormen gemaakt door chemische verwering?  Hoe vlinders de wereld veroverden:een nieuwe 'stamboom' volgt hun 100 miljoen jaar durende reis over de hele wereld
Hoe vlinders de wereld veroverden:een nieuwe 'stamboom' volgt hun 100 miljoen jaar durende reis over de hele wereld
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

