
Wetenschap
Hoe het aantal elektronenschillen in een atoom te bepalen
Door Carter McBride – Bijgewerkt op 24 maart 2022
Het bepalen van het aantal elektronenschillen, of ‘ringen’ rond een atoom, is eenvoudig als je eenmaal het aantal elektronen kent. Elektronenschillen hebben een voorspelbare capaciteit:de eerste bevat twee elektronen, de tweede acht, de derde achttien, enzovoort. Door de schelpen opeenvolgend te vullen, kun je bepalen hoeveel er nodig zijn voor een bepaald element.
Stap 1:Vind het elektronenaantal van het atoom
Raadpleeg het periodiek systeem. Het atoomnummer van een element is gelijk aan het aantal protonen en, voor een neutraal atoom, aan de elektronen. Neon heeft bijvoorbeeld een atoomnummer van 10 en bevat dus tien elektronen.
Stap 2:Vul de eerste schaal
Bereken de capaciteit van een schaal met de formule 2×(n²), waarbij het schaalnummer is. De eerste schil (n=1) kan 2×1²=2 elektronen bevatten. Trek dit af van het totaal aantal elektronen. Bij neon blijven er 10–2=8 elektronen over.
Stap 3:Ga naar de volgende shell
Pas dezelfde formule toe voor de tweede schil (n=2):2×2²=8 elektronen. Omdat de resterende elektronen gelijk zijn aan de capaciteit van de schil, is deze schil vol en zijn er geen elektronen meer over. Neon heeft dus twee elektronenschillen.
Herhaal het proces voor elementen met meer elektronen. Argon (atoomnummer 18) zou bijvoorbeeld twee schillen vullen (2+8=10) en een derde schil nodig hebben (capaciteit 18) om de resterende acht elektronen te huisvesten.
 Op oxide-zeoliet gebaseerd composietkatalysatorconcept maakt syngaschemie mogelijk die verder gaat dan Fischer-Tropsch-synthese
Op oxide-zeoliet gebaseerd composietkatalysatorconcept maakt syngaschemie mogelijk die verder gaat dan Fischer-Tropsch-synthese Koolmonoxide een pure stof of mengsel?
Koolmonoxide een pure stof of mengsel?  Hoe het iso-elektrisch punt te berekenen
Hoe het iso-elektrisch punt te berekenen  Hoe heeft Bohr het Rutherford -model van Atom veranderd?
Hoe heeft Bohr het Rutherford -model van Atom veranderd?  Welke vloeistof en waarom heeft de voorkeur in thermometers?
Welke vloeistof en waarom heeft de voorkeur in thermometers?
 Leeftijd is meer dan een getal:bij kerkuilen laat het zien hoe vatbaar iemand is voor klimaatverandering
Leeftijd is meer dan een getal:bij kerkuilen laat het zien hoe vatbaar iemand is voor klimaatverandering  Eetbare planten die leven in de loofbos
Eetbare planten die leven in de loofbos Zoutvijver op Antarctica, tussen de zoutste wateren op aarde, wordt van onderaf gevoed
Zoutvijver op Antarctica, tussen de zoutste wateren op aarde, wordt van onderaf gevoed Wetenschappers werpen licht op de afdaling van koolstof in de diepe aarde
Wetenschappers werpen licht op de afdaling van koolstof in de diepe aarde Bijgewerkt Exascale-systeem voor simulaties op aarde is sneller dan zijn voorganger
Bijgewerkt Exascale-systeem voor simulaties op aarde is sneller dan zijn voorganger
Hoofdlijnen
- Wetenschappers onthullen superbugs-artillerie
- Wat zijn de overeenkomsten van dierencellen en planten?
- Waarom werd de vastberadenheid van de werkelijke sequentie menselijk genoom beschouwd als beschrijvende wetenschap?
- Waarom planten wereldwijd houtachtig werden
- Organismen wiens cellen geen zichtbare kern hebben?
- Wat komt bij gebruik van de wetenschappelijke methode?
- Endoplasmatisch reticulum:waar is het het meest aanwezig in het lichaam?
- Heeft een schimmelcel de kernstructuur?
- Welke dosis genetisch uniform betekent?
- De sleutel tot het verminderen van de uitstoot van kooldioxide is gemaakt van metaal

- Moleculair dunne interface tussen polymeren voor efficiënt koolstofdioxide-opvangmembraan

- Nieuwe connector voor duurzame constructies op aarde en in de ruimte

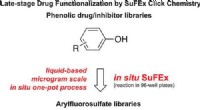
- Click-chemiereacties kunnen de potentie van kankerbestrijdende medicijnen versterken
- Nieuwe tool ontwikkeld om auto-immuunziekten te diagnosticeren en te monitoren
 NASA begint aan vijf Amerikaanse expedities gericht op lucht, land en zee
NASA begint aan vijf Amerikaanse expedities gericht op lucht, land en zee Waar komt de energie die is opgeslagen in koolwaterstoffen vandaan?
Waar komt de energie die is opgeslagen in koolwaterstoffen vandaan?  Waarom ben jij, beste zoöplankton?
Waarom ben jij, beste zoöplankton?  Welk apparaat zet zonne-energie om in elektriciteit?
Welk apparaat zet zonne-energie om in elektriciteit?  Maatstaf voor de kinetische energie van atomen van een object?
Maatstaf voor de kinetische energie van atomen van een object?  Ontbreekt de plantencel een kern?
Ontbreekt de plantencel een kern?  Gefossiliseerde vleugel geeft aanwijzingen over de biodiversiteit van Labradors tijdens het Krijt
Gefossiliseerde vleugel geeft aanwijzingen over de biodiversiteit van Labradors tijdens het Krijt Velcro-methode voor een preciezere binding van medicijndeeltjes
Velcro-methode voor een preciezere binding van medicijndeeltjes
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

