
Wetenschap
Wat is het getal vóór een chemische formule die in een reactievergelijking wordt genoemd?
In een chemische reactievergelijking wordt een getal dat vóór een chemische formule verschijnt een coëfficiënt genoemd . Coëfficiënten worden gebruikt om de vergelijking in evenwicht te brengen, zodat hetzelfde aantal atomen van elk element aan zowel de reactant- als de productzijde verschijnt. Deze praktijk volgt de wet van behoud van massa, die stelt dat massa niet kan worden gecreëerd of vernietigd door een chemische reactie.
Het getal dat rechts van een elementsymbool binnen een formule verschijnt, is een subscript . Subscripts geven het aantal atomen van dat element in de verbinding aan en staan vast; ze kunnen niet worden gewijzigd bij het balanceren van een vergelijking.
Een eenvoudige reactie in evenwicht brengen:waterstof en zuurstof vormen water
Ongebalanceerde vergelijking:H2 + O2 → H2 O
Stap 1 – Pas de productzijde aan:H2 + O2 → 2H2 O
Stap 2 – Breng waterstofatomen in evenwicht:2H2 + O2 → 2H2 O
Resultaat:Vier waterstofatomen en twee zuurstofatomen aan beide kanten, dus de vergelijking is in evenwicht.
Algemene stappen voor het balanceren van chemische vergelijkingen
1. Identificeer de meest complexe verbinding
Kies een element dat in één samenstelling aan één kant van de vergelijking verschijnt. Voeg een coëfficiënt toe aan die verbinding om het aantal atomen van dat element aan beide kanten gelijk te maken.
2. Breng polyatomaire ionen in evenwicht als hele eenheden
Houd ionen zoals NO3 vast - of CO3 2- intact. Bijvoorbeeld:
Onevenwichtig:Ca + HNO3 → H2 + Ca(NO3 )2
Evenwichtig:Ca + 2HNO3 → H2 + Ca(NO3 )2
3. Breng de resterende elementen in evenwicht
Pas na het hanteren van de complexe soorten de coëfficiënten voor eventuele resterende elementen aan. Voor verbranding van heptaan:
Ongebalanceerd:C7 H16 + O2 → CO2 + H2 O
Evenwichtig:C7 H16 + 11O2 → 7CO2 + 8H2 O
4. Verifieer uw werk
Tel elk element aan beide kanten om de gelijkheid te bevestigen. Voor complexe vergelijkingen kunt u overwegen een tabel te maken om het aantal atomen bij te houden.
kivitimof/iStock/GettyImages
 Dodelijke bosbranden in Californië verwoesten schilderachtige rivierstad
Dodelijke bosbranden in Californië verwoesten schilderachtige rivierstad Licht werpen op hoeveel koolstof tropische bossen kunnen absorberen
Licht werpen op hoeveel koolstof tropische bossen kunnen absorberen Veranderende winden bieden hoop voor bosbranden in Californië
Veranderende winden bieden hoop voor bosbranden in Californië Natuurbrand bestrijden met GPS-gegevens
Natuurbrand bestrijden met GPS-gegevens Onderzoekers kijken om te zien hoe verheven woningen in Florida bestand zijn tegen orkaan Michael
Onderzoekers kijken om te zien hoe verheven woningen in Florida bestand zijn tegen orkaan Michael
Hoofdlijnen
- Hoe zijn organismen manier van leven geroepen?
- Hoe evolutionisten bepalen of twee organismen een gemeenschappelijke voorouder delen?
- Waarom zijn er variaties in eigenschappen?
- Wie presenteerde de celtheorie?
- Hoe maken eukaryotische cellen meer cellen?
- Wat is een FLASK-definitie?
- Symbiosestudie legt nieuwe oorsprongstheorieën bloot en identificeert experimentele systemen voor het plantenleven
- Wat is de urine -pH bij een uitgedroogde persoon?
- De pathogeen kan het lichaam op welke van de volgende manieren het lichaam betreden?
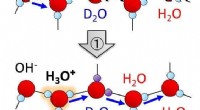
- Unieke structurele fluctuaties aan het ijsoppervlak bevorderen auto-ionisatie van watermoleculen
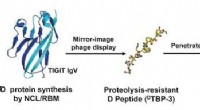
- Checkpointblokkade door een D-peptide voor kankerimmunotherapie
- MOF's kunnen lastige gassen detecteren en sorteren

- Analyse van magnetische materialen was nog nooit zo begrijpelijk

- Katalysatoronderzoek voor zonnebrandstoffen:amorf molybdeensulfide werkt het beste

 Nucleïnezuren:structuur, functie en belang
Nucleïnezuren:structuur, functie en belang  Wat is het punt van binnenkomst van koolstofdioxide in de planten van de binnenkant van de bladeren?
Wat is het punt van binnenkomst van koolstofdioxide in de planten van de binnenkant van de bladeren?  Hoe wind het Antarctische zee-ijs helpt groeien, zelfs als het Noordpoolgebied smelt
Hoe wind het Antarctische zee-ijs helpt groeien, zelfs als het Noordpoolgebied smelt  Uit onderzoek blijkt hoe groene ruimte gewelddadige criminaliteit kan terugdringen
Uit onderzoek blijkt hoe groene ruimte gewelddadige criminaliteit kan terugdringen  Van allelen tot uiterlijk:de wetenschap achter genetische expressie
Van allelen tot uiterlijk:de wetenschap achter genetische expressie  Klimaatverandering vereist hetzelfde leiderschap als COVID-19, en Australië faalt
Klimaatverandering vereist hetzelfde leiderschap als COVID-19, en Australië faalt Waarom is de energiestroom in een ecosysteem beschreven als één manier?
Waarom is de energiestroom in een ecosysteem beschreven als één manier?  Wat is de heetste ster in het universum?
Wat is de heetste ster in het universum?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

