
Wetenschap
Hoe ongunstige pH-niveaus de enzymactiviteit beïnvloeden
CIPhotos/iStock/GettyImages
Enzymen zijn de katalysatoren van het leven en drijven vrijwel elke chemische reactie aan die biologische systemen in stand houdt. Hun activiteit is zeer gevoelig voor de omgeving, met name de pH, die de driedimensionale structuur van het enzym en daarmee de functie ervan kan veranderen.
TL;DR
Enzymen – gespecialiseerde eiwitten – drijven de meeste biochemische reacties aan. Elk heeft een specifieke optimale pH. Afwijken van dit ideale bereik kan de activiteit vertragen of stopzetten, soms onomkeerbaar.
Wat is een enzym?
Enzymen zijn polypeptideketens die zijn samengesteld uit aminozuren. Hun unieke volgorde bepaalt hoe de ketting zich in een specifieke driedimensionale vorm vouwt. Deze conformatie creëert een actieve plaats die substraten bindt, waardoor reacties worden versneld door de activeringsenergie te verlagen. De lokale pH beïnvloedt de ionisatietoestand van de zijketens van aminozuren, waardoor het enzym een nieuwe vorm kan krijgen en de katalytische efficiëntie ervan kan worden beïnvloed.
Chemische effecten van pH
De pH-schaal weerspiegelt de concentratie vrije waterstofionen (H⁺) of hydroxide-ionen (OH⁻) in een oplossing. Verschuivingen in de pH zorgen ervoor dat ioniseerbare groepen binnen aminozuren protonen winnen of verliezen, wat leidt tot veranderingen in de ladingsverdeling. Deze veranderingen kunnen waterstofbruggen, elektrostatische interacties en disulfidebruggen verstoren die de structuur van het enzym stabiliseren, wat resulteert in een conformationele verandering die vaak de katalytische activiteit vermindert.
Enzymprestatieveranderingen
Elk enzym heeft een optimale pH waarbij het met maximale efficiëntie werkt, ervan uitgaande dat andere omstandigheden, zoals temperatuur en substraatconcentratie, ook ideaal zijn. Pepsine, een spijsverteringsenzym in de maag, functioneert bijvoorbeeld het beste rond een pH van 2, terwijl bloedenzymen zoals lactaatdehydrogenase een piek bereiken bij een neutrale pH van 7,4. Wanneer de omgeving buiten de optimale pH van een enzym komt, neemt de activiteit doorgaans geleidelijk af, en bij extreme afwijkingen kan het enzym gedenatureerd raken, waardoor het zijn functionele vorm permanent verliest of totdat de omstandigheden terugkeren.
Andere factoren die enzymen beïnvloeden
Naast de pH oefent de temperatuur een vergelijkbare invloed uit op de enzymstructuur, waarbij elk enzym een duidelijk temperatuuroptimum heeft. De substraatconcentratie bepaalt ook de reactiesnelheid:het verhogen van de substraatniveaus versnelt de reactie totdat het enzym verzadigd raakt, waarna de snelheid een plateau bereikt. Enzymremmers (moleculen die zich aan de actieve plaats of elders binden) kunnen de katalyse blokkeren, terwijl productremming (feedback) de enzymactiviteit automatisch naar beneden reguleert wanneer voldoende product zich ophoopt.
 Hoeveel mol zwavelatomen zijn aanwezig in 3,00 CS2?
Hoeveel mol zwavelatomen zijn aanwezig in 3,00 CS2?  Chemische versus fysische reacties:het verschil begrijpen
Chemische versus fysische reacties:het verschil begrijpen  Waarom is het moeilijker om een binnenste shell -elektron te verwijderen dan een valentie uit het atoom?
Waarom is het moeilijker om een binnenste shell -elektron te verwijderen dan een valentie uit het atoom?  Hoeveel elektronen van een calciumatoom zijn betrokken bij chemische binding?
Hoeveel elektronen van een calciumatoom zijn betrokken bij chemische binding?  Een heldere halfgeleider op basis van tin zou de opwekking van zonne-energie kunnen verbeteren
Een heldere halfgeleider op basis van tin zou de opwekking van zonne-energie kunnen verbeteren
Hoofdlijnen
- 10 historische medische praktijken die ooit als legitiem werden beschouwd – lessen voor de moderne geneeskunde
- Wat zijn de overeenkomsten en verschillen in wetenschapstakken?
- Wat zijn 2 hoofdtypen dieren?
- Wat hondeneigenaren moeten weten over leptospirose
- Nieuwe aanwijzingen waarom mutaties in het MYH9-gen een breed spectrum aan aandoeningen bij mensen veroorzaken
- Welk orgaan staat bekend als chemisch laboratorium in het menselijk lichaam?
- Wat groeit meer bacteriënbouillon of agar?
- Ziekte in het vuil:hoe schurftveroorzakende mijten een Tasmaanse wombatpopulatie hebben gedecimeerd
- Wat is kale kernen?
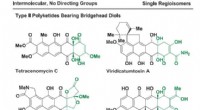
- Metaalgekatalyseerde toevoeging van verzadigde koolstof aan CC-bindingen:een relevante reactie voor de synthese van type II polyketiden
- Hoe restwarmte-energie op te vangen met verbeterde polymeren
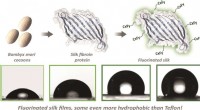
- Wetenschappers gebruiken gemodificeerde zijde-eiwitten om nieuwe anti-aanbakoppervlakken te creëren
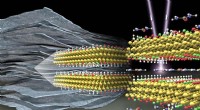
- Snel en furieus:nieuwe klasse van 2D-materialen slaat elektrische energie op
- Techniek maakt afdrukbare en herschrijfbare kleurenafbeeldingen mogelijk
 De vergelijking voor de enkele verplaatsingsreactie tussen broom en calciumjodide?
De vergelijking voor de enkele verplaatsingsreactie tussen broom en calciumjodide?  Welk type cel moet een mutatie bevatten om te worden doorgegeven van vrouwen haar nakomelingen?
Welk type cel moet een mutatie bevatten om te worden doorgegeven van vrouwen haar nakomelingen?  Hoe internationaal toerisme en reizen een manier kunnen zijn om invasieve soorten te introduceren
Hoe internationaal toerisme en reizen een manier kunnen zijn om invasieve soorten te introduceren Hoe pittig wordt mosterd afhankelijk van de grondsoort?
Hoe pittig wordt mosterd afhankelijk van de grondsoort?  Wat at Megalodon? Alles wat het wilde, inclusief andere roofdieren
Wat at Megalodon? Alles wat het wilde, inclusief andere roofdieren  Elektriciteit opslaan in papier:een organische gemengde ion-elektronengeleider voor vermogenselektronica
Elektriciteit opslaan in papier:een organische gemengde ion-elektronengeleider voor vermogenselektronica Miljoenen boeren vullen 's werelds grootste delta aan
Miljoenen boeren vullen 's werelds grootste delta aan De Rode Zee is vernoemd naar de algenbloei van wat?
De Rode Zee is vernoemd naar de algenbloei van wat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

