
Wetenschap
Hoe elementen te combineren om verbindingen te vormen:een praktische gids
Door Mara Pesacreta
Bijgewerkt op 30 augustus 2022
JeffreyRasmussen/iStock/GettyImages
Begrijpen hoe elementen uit het periodiek systeem zich verenigen om verbindingen te creëren, is van fundamenteel belang voor de chemie. De unieke eigenschappen van elk element bepalen hoe het zich hecht, hetzij door metallische, ionische of covalente interacties. Door deze principes onder de knie te krijgen, kunnen scheikundigen het gedrag van stoffen in wetenschappelijke en industriële contexten voorspellen en manipuleren.
Stap 1:Identificeer metalen, niet-metalen en metalloïden
Metalen bevinden zich links en in het midden van het periodiek systeem en blinken uit als elektrische geleiders; koper is een klassiek voorbeeld. Metalloïden zoals boor, silicium, germanium, arseen, antimoon, tellurium en polonium vertonen gemengde kenmerken, waardoor metallisch en niet-metaalachtig gedrag wordt overbrugd. Niet-metalen, te vinden aan de rechterkant (exclusief waterstof), zijn meestal gassen of broze vaste stoffen en geleiden elektriciteit slecht; stikstof is een voorbeeld van deze groep.
Stap 2:Herken metaalverbindingen
Wanneer identieke metaalatomen zich combineren, vormen ze metaalbindingen. In deze opstelling worden valentie-elektronen gedelokaliseerd over een rooster, waardoor een vrije elektronenstroom mogelijk wordt; zink demonstreert dit fenomeen.
Stap 3:Overweeg elementen met hoge elektronegativiteit
Halogenen in Groep 17 bezitten zeven valentie-elektronen, waardoor ze zeer elektronegatief zijn. Hun sterke aantrekkingskracht op elektronen stimuleert de vorming van ionische of covalente bindingen, afhankelijk van het partnerelement.
Stap 4:Overweeg elementen met een lage elektronegativiteit
Alkalimetalen in Groep 1 hebben één valentie-elektron, wat resulteert in de laagste elektronegativiteitswaarden. Deze elementen doneren gemakkelijk elektronen tijdens binding.
Stap 5:Metaal-niet-metaalinteracties leveren ionische bindingen op
Wanneer een metaal met een lage elektronegativiteit een niet-metaal met een hoge elektronegativiteit ontmoet, vindt er elektronenoverdracht plaats, waardoor een ionenrooster ontstaat. Kaliumchloride (KCl) is een schoolvoorbeeld van een dergelijke verbinding.
Stap 6:Niet-metaal-niet-metaalbindingen vormen covalente structuren
Het combineren van twee of meer niet-metalen leidt doorgaans tot covalente bindingen met gedeelde elektronen, zoals te zien is in stikstofdioxide (NO₂). Deze moleculen vertonen vaak gerichte binding en een gedefinieerde moleculaire geometrie.
Stap 7:Onderscheid organische van anorganische verbindingen
De organische chemie richt zich op koolstofhoudende moleculen. Methaan (CH₄) illustreert een organische verbinding, terwijl magnesiumbromide (MgBr₂) een puur anorganisch zout vertegenwoordigt.
Hulpmiddelen die je nodig hebt
- Computer
- Scheikundeleerboek
- Referentie periodiek systeem
- Pen
- Papier
 Onderzoek toont aan waarom er een goede diepte is voor ondergrondse magmakamers
Onderzoek toont aan waarom er een goede diepte is voor ondergrondse magmakamers Wat klinkt vogels bang maken?
Wat klinkt vogels bang maken?  De koolstofemissies als gevolg van de vernietiging van mangrovebossen zullen naar verwachting tegen het einde van de eeuw met 50.000% toenemen
De koolstofemissies als gevolg van de vernietiging van mangrovebossen zullen naar verwachting tegen het einde van de eeuw met 50.000% toenemen  Osmose-experimenten met Gummy Bears
Osmose-experimenten met Gummy Bears Hebben we een IPCC nodig voor voedsel?
Hebben we een IPCC nodig voor voedsel?
Hoofdlijnen
- Wat doen cellen met ATP?
- Wat regelt welke stoffen in en uit cellen gaan?
- Waar krijgen organismen hun DNA?
- Rol van het organisme in zijn ecosysteem?
- Toezichthouders overwegen wat ze moeten doen aan het ingestorte kreeftenbestand
- Hoe uw immuunsysteem werkt
- Wat zijn feiten die de evolutie weerleggen?
- Welke omgevingsfactoren gaven waarschijnlijk de voorkeur aan de evolutie van autotrofen?
- Hoe worden de spiercellen gerangschikt ten opzichte van elkaar?
- Snelle manier om moleculaire kooien te maken, kan het zoeken naar nieuwe materialen vernieuwen
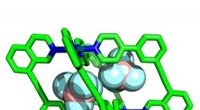
- Wetenschappers maken membranen voor omgekeerde osmose met instelbare dikte
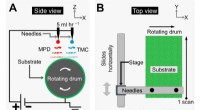
- Nieuw protocol voor het meten van achtergrondniveaus van drugs in misdaadlabs

- Toegang openen om de synthetische chemie van neptunium te verkennen
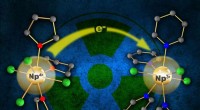
- Nieuwe technologie voor eiwitbioconjugatie en structurele proteomics
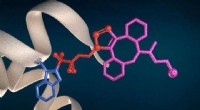
 Grindr geeft toe aan de reacties van gebruikers, maar respecteert het zijn gebruikers?
Grindr geeft toe aan de reacties van gebruikers, maar respecteert het zijn gebruikers?  Wat is een geleider van elektriciteit en een isolator -elektriciteit?
Wat is een geleider van elektriciteit en een isolator -elektriciteit?  Welke wet beweert dat energie ook in aanmerking komt?
Welke wet beweert dat energie ook in aanmerking komt?  Vlieg me (gedeeltelijk) naar de maan
Vlieg me (gedeeltelijk) naar de maan Het achtergrondgezoem van de ruimte zou verborgen zwarte gaten kunnen onthullen
Het achtergrondgezoem van de ruimte zou verborgen zwarte gaten kunnen onthullen Is seks in de eerste plaats een strategie tegen overdraagbare kanker?
Is seks in de eerste plaats een strategie tegen overdraagbare kanker?  Wat zijn de namen van sterren in Little Dipper?
Wat zijn de namen van sterren in Little Dipper?  Wat is de conceptkaart van de fysica en zijn takkensubwijken?
Wat is de conceptkaart van de fysica en zijn takkensubwijken?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

