
Wetenschap
Beheersing van skeletvergelijkingen:stapsgewijze handleiding voor het in evenwicht brengen van chemische reacties
Door Grant D. McKenzie • Bijgewerkt 30 augustus 2022
Scheikundestudenten gebruiken routinematig skeletvergelijkingen als een fundamenteel hulpmiddel voor het in evenwicht brengen van reacties. De reactanten staan aan de linkerkant, de producten aan de rechterkant, en een pijl verbindt ze, waardoor de vergelijking zijn ‘skelet’-structuur krijgt. Om de vergelijking te voltooien, moeten de juiste stoichiometrische coëfficiënten worden bepaald, die de relatieve hoeveelheden van elke soort aangeven.
Stap 1:Lijst van de reactanten
Identificeer alle reactanten en plaats ze aan de linkerkant, gescheiden door plustekens. Volg de reactanten met een reactiepijl. Als calciumchloride en natriumsulfaat bijvoorbeeld reageren, schrijf dan:
CaCl2 + Na2 SO4 →
Stap 2:Schrijf de producten
Plaats de bijbehorende producten aan de rechterkant van de pijl, wederom gescheiden door plustekens. In het bovenstaande voorbeeld zijn de producten calciumsulfaat en natriumchloride:
CaCl2 + Na2 SO4 → CaSO4 + NaCl
In dit stadium is de vergelijking nog steeds een skelet, omdat de aantallen natrium- en chlooratomen aan beide kanten niet overeenkomen.
Stap 3:statussymbolen toevoegen
Toestandssymbolen verduidelijken de fysieke toestand van elke verbinding:vaste stof (s), vloeistof (l), gas (g) of waterige oplossing (aq). In ons voorbeeld vormen twee waterige oplossingen samen een waterige oplossing en een vast neerslag:
CaCl2 (aq) + Na2 SO4 (aq) → CaSO4 (s) + NaCl (aq)
Nu de toestandssymbolen op hun plaats staan, is de skeletvergelijking klaar voor het in evenwicht brengen van de coëfficiënten, waardoor massabehoud tijdens de reactie wordt gegarandeerd.
Deze stappen bieden een duidelijk raamwerk voor het construeren van skeletvergelijkingen voordat algebraïsche methoden worden toegepast om ze in evenwicht te brengen.
 Welk metaal is meer reactief neon of koper?
Welk metaal is meer reactief neon of koper?  Wat is de naam van ternair zuur gevormd met chloor dat de minste zuurstofatomen heeft?
Wat is de naam van ternair zuur gevormd met chloor dat de minste zuurstofatomen heeft?  Bacteriële cellen zure kleurstoffen dragen welke lading?
Bacteriële cellen zure kleurstoffen dragen welke lading?  Dankzij de techniek voor het bewerken van genen kunnen zijderupsen spinnenzijde produceren
Dankzij de techniek voor het bewerken van genen kunnen zijderupsen spinnenzijde produceren Wat is de relatie tussen de sterkte van de metaalbinding en de verdampingsenthalpie?
Wat is de relatie tussen de sterkte van de metaalbinding en de verdampingsenthalpie?
 Studie:Inheemse volkeren bezitten of beheren ten minste een kwart van het landoppervlak ter wereld
Studie:Inheemse volkeren bezitten of beheren ten minste een kwart van het landoppervlak ter wereld Is een koolstofvrije,
Is een koolstofvrije,  Rechtszaak:3M-besmetting leidde tot meer kanker, onvruchtbaarheid
Rechtszaak:3M-besmetting leidde tot meer kanker, onvruchtbaarheid Wat maakt een bosbrand in Californië het ergst? Sterfgevallen en grootte
Wat maakt een bosbrand in Californië het ergst? Sterfgevallen en grootte Wat staat bekend als de vegetatie op een grotere breedtoze vlakte?
Wat staat bekend als de vegetatie op een grotere breedtoze vlakte?
Hoofdlijnen
- Wat is een zelfstandig naamwoord voor eiwitten?
- Hoe creëer je een hypothese over wetenschappelijk probleem?
- Wat biedt ondersteuning voor cel en heeft twee subdelen?
- Wat zijn de niveaus van biologische organisaties in orde van de kleinste tot de grootste?
- In gewervelde diercellen waar komt de synthese van melkzuur op?
- Wat is de belangrijkste functie van Nucleolus?
- Wat is de definitie van massa in de biologie?
- Hoe menselijke eieren eindigen met het verkeerde aantal chromosomen
- Onderzoekers ontdekken dat de celcortex wordt geactiveerd door duizenden kortlevende eiwitcondensaten
- Voor fotokatalysatoren, de tand des tijds doorstaan betekent een perfecte partner vinden

- Doorbraak voor het volgen van RNA met fluorescentie
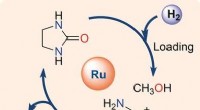
- Chemisch waterstofopslagsysteem
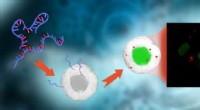
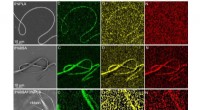
- Biofysici mengen onverenigbare componenten tot één nanovezel
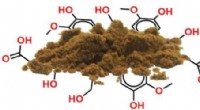
- Kunststof van hout? Röntgenanalyse wijst de weg naar op lignine gebaseerde componenten op maat
 Een instrument dat wordt gebruikt om het vriespunt van een stof te meten?
Een instrument dat wordt gebruikt om het vriespunt van een stof te meten?  Weten geavanceerde beschavingen dat we hier zijn?
Weten geavanceerde beschavingen dat we hier zijn?  Wat resulteert in radioactief verval en veroorzaakt verlies van een of meer protonen?
Wat resulteert in radioactief verval en veroorzaakt verlies van een of meer protonen?  Zwavelanalyse ondersteunt de timing van het verschijnen van zuurstof
Zwavelanalyse ondersteunt de timing van het verschijnen van zuurstof De hoge luchtvervuiling in Denemarken kan de academische prestaties van kinderen beïnvloeden
De hoge luchtvervuiling in Denemarken kan de academische prestaties van kinderen beïnvloeden  Hoogwaardige anode voor all-solid-state lithiumbatterijen is gemaakt van silicium nanodeeltjes
Hoogwaardige anode voor all-solid-state lithiumbatterijen is gemaakt van silicium nanodeeltjes Een milieuvriendelijkere airconditioner
Een milieuvriendelijkere airconditioner Een vierkant heeft een omtrek van 36 inch. Wat is het gebied?
Een vierkant heeft een omtrek van 36 inch. Wat is het gebied?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

