
Wetenschap
Hoe u de moleculaire polariteit kunt bepalen:een stapsgewijze handleiding
Door Arthur Ramsay
Bijgewerkt op 30 augustus 2022
Polariteit in de chemie beschrijft hoe ongelijkmatig elektronen worden verdeeld tussen atomen in een binding. Wanneer elektronen meer tijd dichter bij één atoom doorbrengen, wordt dat atoom gedeeltelijk negatief terwijl het andere gedeeltelijk positief wordt, waardoor een dipool ontstaat. Dit principe ligt ten grondslag aan veel alledaagse verschijnselen – van de oplosmiddeleigenschappen van water tot het gedrag van biomoleculen. Volgens onderzoek van de Universiteit van Arizona heeft water een gedeeltelijke negatieve lading nabij het zuurstofatoom en een gedeeltelijke positieve lading nabij de waterstofatomen .
Stap 1:Teken de Lewis-structuur
Begin met het schetsen van de Lewis-structuur van je molecuul. Identificeer elk aanwezig element, aangezien de geometrie van het molecuul invloed heeft op hoe dipolen optellen.
Stap 2:Elektronegativiteit opzoeken
Raadpleeg een betrouwbare elektronegativiteitstabel om de elektronegativiteitswaarde voor elk element in het molecuul te vinden.
Stap 3:Bereken de verschillen in elektronegativiteit
Trek de elektronegativiteit van het ene atoom in een binding af van die van het andere en neem de absolute waarde. Gebruik de volgende drempelwaarden:
- 0,0 – 1,2:niet-polaire binding
- 1,2 – 1,8:polaire covalente binding
- ≥1,8:ionbinding
Stap 4:Herhaal voor elke binding
Pas de berekening toe op elke binding in het molecuul om de individuele polariteit ervan te bepalen.
Stap 5:Visualiseer dipoolrichtingen
Plaats een pijl op elke polaire binding, wijzend naar het meer elektronegatieve atoom. Als alle pijlen naar één enkel centrum convergeren, heffen de dipolen elkaar op en is het molecuul over het algemeen niet-polair. Als de pijlen elkaar niet tegenhouden, bezit het molecuul een netto dipoolmoment en is het polair.
Waarschuwing
Elektronegativiteitswaarden kunnen verschuiven afhankelijk van de chemische omgeving; elementen zoals fluor kunnen verschillende waarden vertonen wanneer ze aan verschillende partners zijn gebonden. Houd altijd rekening met de specifieke bindingscontext bij het toepassen van deze regels.
 Molaliteit berekenen:een stapsgewijze handleiding met NaCl-voorbeeld
Molaliteit berekenen:een stapsgewijze handleiding met NaCl-voorbeeld  Wat is de molariteit van een oplossing die is bereid door 2,41 g kaliumjodide ki in 100 ml water op te lossen?
Wat is de molariteit van een oplossing die is bereid door 2,41 g kaliumjodide ki in 100 ml water op te lossen?  Belang van het drogen van organische vloeistoffen vóór IR-spectroscopie
Belang van het drogen van organische vloeistoffen vóór IR-spectroscopie  Staat roestvrij staal op het periodiek systeem?
Staat roestvrij staal op het periodiek systeem?  Wat wordt gemaakt als 2 atomen combineren?
Wat wordt gemaakt als 2 atomen combineren?
Hoofdlijnen
- Wat zijn de kleine organismen die je een microscoop nodig hebt om te zien?
- Hoe is een arts gerelateerd aan de wetenschap?
- Welke microscopische structuren voeren de belangrijkste levensfuncties uit?
- Wat is de naam van de interne secretoire klieren van de wetenschap?
- Hoe de taal die u spreekt aansluit bij uw genetische afkomst en van invloed kan zijn op onderzoek naar de gezondheid
- Zonder replicatie -organismen konden niet met succes doen wat?
- Heeft het herschikken van chromosomen invloed op hun functie?
- Welke rol spelen anti-oxidanten specifiek in het menselijk lichaam en op de hersenen?
- Hoe ziet een wetenschappelijke variabele eruit?
- Wetenschappers vinden een manier om langlevende, snelladende batterijen
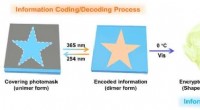
- Nieuwe fluorescerende organohydrogel voorgesteld om dubbele informatie-encryptie te bereiken
- Mineraal ondergaat zelfgenezing van stralingsschade

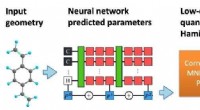
- Doorbraak gemeld in door machine learning verbeterde kwantumchemie
- Nieuw onderzoek levert supersterke aluminiumlegering op

 Welke vorm zou een molecuul met vier atomen eromheen hebben?
Welke vorm zou een molecuul met vier atomen eromheen hebben?  Welke twee krachten vertragen een raket naar beneden?
Welke twee krachten vertragen een raket naar beneden?  Succesvolle Egg Drop-ideeën
Succesvolle Egg Drop-ideeën Podcasters vinden niche in de Arabische wereld
Podcasters vinden niche in de Arabische wereld In welke twee aardgebieden is zuurstof het tweede meest voorkomende element per volume?
In welke twee aardgebieden is zuurstof het tweede meest voorkomende element per volume?  Celstructuur en -functie:onderzoek naar de relatie
Celstructuur en -functie:onderzoek naar de relatie  Continentale interieurs zijn misschien niet zo tektonisch stabiel als geologen denken
Continentale interieurs zijn misschien niet zo tektonisch stabiel als geologen denken Wat is elektrisch neutrale materie?
Wat is elektrisch neutrale materie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

