
Wetenschap
Atomaire binding begrijpen:typen, mechanismen en betekenis
Door Emily Martinez Bijgewerkt op 30 augustus 2022
Atoombinding is chemische binding. Chemische binding is het fysieke proces dat verantwoordelijk is voor de interacties tussen atomen en moleculen. Obligaties lopen sterk uiteen; er zijn covalente, ionische, waterstof-, metallische en vele andere soorten bindingen, en ze hebben allemaal een werkende verbinding in alle levende wezens. Er zijn twee verschillende soorten atomaire bindingen; primair en secundair. De primaire bindingen produceren chemische bindingen die atomen bij elkaar houden.
Soorten atomaire obligaties
Soorten atomaire obligaties
Atoomobligaties hebben twee soorten obligaties; primaire en secundaire bindingen, en de primaire bindingen hebben drie soorten bindingen:metallisch, covalent en ionisch. De secundaire obligaties zijn ook subsecties van obligaties en worden beschouwd als de zwakkere elementen.
Metaalbinding
Metaalbinding
Metaalbindingen zijn een metaal en delen buitenste bindingen met atomen in een vaste stof. Elk atoom geeft een positieve lading af door zijn buitenste elektronen af te werpen, en de negatief geladen elektronen houden de metaalatomen bij elkaar.
Ionische binding
Ionische binding
Atomen zijn gevuld met een buitenste schil van elektronen. Elektronenschillen worden gevuld door elektronen van het ene atoom naar het andere over te brengen. Donoratomen zullen een positieve lading aannemen, en de acceptoren zullen een negatieve lading hebben. Ze zullen elkaar aantrekken door positief en negatief te zijn, en er zal dan een band ontstaan.
Covalente obligaties
Covalente obligaties
Atomen delen graag hun elektronen en dit zorgt ervoor dat hun buitenste schil compleet is. Een covalente binding ontstaat door het delen van atomen en elektronen. Dit levert een sterke covalente binding op.
Secundaire obligaties
Secundaire obligaties
Secundaire bindingen zijn aanzienlijk zwakker dan primaire bindingen, omdat ze vaak zwakke schakels produceren en vervormingen in de binding veroorzaken. Secundaire bindingen omvatten waterstof- en van der wals-bindingen.
Waterstofbruggen
Waterstofbruggen
Een gemeenschappelijke binding is een waterstofbinding. Ze komen het meest voor in covalent gebonden moleculen die waterstof bevatten. Waterstofbindingen delen tussen covalente en zuurstofrijke atomen. Dit leidt tot zeer kleine elektrische ladingen rond de waterstofbruggen en negatieve ladingen rond de zuurstofverbindingen.
Van der Waals Obligaties
Van der Waals Obligaties
Van der Waals-obligaties zijn de zwakste bindingen, maar het zijn ongelooflijk belangrijke gassen, die bij lage temperaturen worden gekoeld. Deze bindingen worden gecreëerd door kleine ladingen van positieve en negatieve elektronen die een zwakke binding produceren. Van der Waals-obligaties worden overweldigd door thermische energie, waardoor ze niet meer goed functioneren.
 Zijn de meeste patronen in de natuur onregelmatige patronen?
Zijn de meeste patronen in de natuur onregelmatige patronen?  Planetaire golven, afgesneden dieptepunten en blokkerende hoogtepunten:wat zit er achter recordoverstromingen op het zuidelijk halfrond?
Planetaire golven, afgesneden dieptepunten en blokkerende hoogtepunten:wat zit er achter recordoverstromingen op het zuidelijk halfrond? Wat zijn de oorzaken van ecologiecale problemen?
Wat zijn de oorzaken van ecologiecale problemen?  Robots kunnen een revolutie teweegbrengen in de monitoring van het mariene milieu
Robots kunnen een revolutie teweegbrengen in de monitoring van het mariene milieu Wat is een stofdoeleinden?
Wat is een stofdoeleinden?
Hoofdlijnen
- Wat zijn twee voorbeelden van nucleïnezuren?
- Waarom is de studie van milieubiologie noodzakelijk of belangrijk voor mensen?
- Wat moet wetenschapper weten dat een wetenschapper is?
- Ideeën voor een Sunscreen Science Fair Project
- De Saguaro Cactus is een iconisch symbool van het Amerikaanse zuidwesten
- De belangrijkste soorten flora en fauna gevonden in aquatische ecosystemen worden voornamelijk bepaald door?
- Wat is de functie van de amature -plant?
- Archaeoraptor:de hoax die de verbinding tussen dinosauriërs en vogels bijna ondermijnde
- Waarom de meeste virussen die bacteriën infecteren, hebben staarten, terwijl dieren en planten dat niet doen?
- Video:Hoe kom je van die stinkdiergeur af?

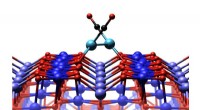
- Onderzoek naar mono-atomaire platinakatalysatoren
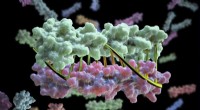
- Wetenschappers programmeren eiwitten om precies te paren
- Team ontwikkelt adhesiesysteem voor meerdere oppervlakken, gemodelleerd naar sprinkhanenvoeten

- Onderzoek onthult het eerste niet-centrosymmetrische fluoroxosilicofosfaat met Si-F-bindingen
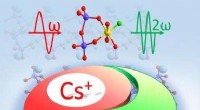
 Wat zijn de voor- en nadelen van beryllium?
Wat zijn de voor- en nadelen van beryllium?  Wat is hemaprodiaat?
Wat is hemaprodiaat?  Wanneer is potentiële energie 0?
Wanneer is potentiële energie 0?  Wat wij een ASRTONOMICAL -eenheid?
Wat wij een ASRTONOMICAL -eenheid?  Kenmerken van nucleïnezuren
Kenmerken van nucleïnezuren Inzicht in pH en zuurgraad:hoe verandert de pH met de zuurgraad?
Inzicht in pH en zuurgraad:hoe verandert de pH met de zuurgraad?  De aarde en korst is een dunne laag die bestaat uit?
De aarde en korst is een dunne laag die bestaat uit?  Wat is de chemische samenstelling van chromatine?
Wat is de chemische samenstelling van chromatine?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

