
Wetenschap
Massapercentage berekenen:een stapsgewijze handleiding
Door Oxana Fox • 29 april 2023 12:10 uur EST
Wat is massapercentage?
Het massapercentage drukt de concentratie van een opgeloste stof uit ten opzichte van de totale massa van een oplossing. Het wordt berekend als een percentage van de massa van de opgeloste stof gedeeld door de massa van de gehele oplossing.
De massa-percentageformule
Om de massapercentage-samenstelling van een verbinding in een mengsel te bepalen, gebruik je:
Massapercentage =\(\frac{a}{M} \times 100\)waar een is de massa van de opgeloste stof en M is de totale massa van de oplossing (opgeloste stof + oplosmiddel).
Voorbeeld:massapercentage berekenen
Stel dat 10 g natriumchloride (NaCl) en 6 g natriumbicarbonaat (NaHCO₃) worden opgelost in 120 g water. De totale oplossingsmassa is:
\(M =10\text{ g} + 6\text{ g} + 120\text{ g} =136\text{ g}\)
Massapercentage NaCl:
\(\frac{10\text{ g}}{136\text{ g}} \times 100\% =7,35\%\)
Massapercentage NaHCO₃:
\(\frac{6\text{ g}}{136\text{ g}} \times 100\% =4,41\%\)
Waarom massapercentage belangrijk is
Met massapercentage kunnen scheikundigen de relatieve bijdragen van elke component in een mengsel kwantificeren, wat helpt bij reactieontwerp, kwaliteitscontrole en analytische berekeningen. Bijvoorbeeld het bepalen van de elementaire samenstelling van glucose of de concentratie van opgeloste stoffen in farmaceutische formuleringen.
Verbinding met molaire massa
Molaire massa, de massa van één mol van een stof, is gerelateerd aan het massapercentage bij het omrekenen tussen massa en molhoeveelheden:
M =\(\frac{m}{n}\)
waar M is de molaire massa (kgmol⁻¹), m is de massa van de stof, en n is het aantal mol.
TL;DR
Een mol is gelijk aan het aantal atomen of moleculen van Avogadro. Hoewel het aantal deeltjes voor elk element hetzelfde is, verschilt de massa omdat elk atoom een verschillend atoomgewicht heeft.
 Hoe sociale media kustgebieden helpen omgaan met de kracht van extreme stormen
Hoe sociale media kustgebieden helpen omgaan met de kracht van extreme stormen  Het belang van fossielen
Het belang van fossielen  Zuurstof bestuderen, wetenschappers ontdekken aanwijzingen voor herstel van massale uitsterving
Zuurstof bestuderen, wetenschappers ontdekken aanwijzingen voor herstel van massale uitsterving Australië verandert van verdediging in aanval in natuurbrandgevecht
Australië verandert van verdediging in aanval in natuurbrandgevecht Het onderzoeksteam ontwikkelt een impactgebaseerd voorspellingssysteem voor verbeterde vroegtijdige waarschuwing voor overstromingen
Het onderzoeksteam ontwikkelt een impactgebaseerd voorspellingssysteem voor verbeterde vroegtijdige waarschuwing voor overstromingen
Hoofdlijnen
- Onderzoek onderzoekt hoe de oppervlakken van borstimplantaten de immuunrespons beïnvloeden
- Wat kan een dubbele gen produceren?
- Waarom zijn zoveel levende dingen afhankelijk van plantachtige protist?
- Hoe is schimmels anders dan dieren en planten?
- Hoe onderzoekers een decennia-oud mysterie met betrekking tot celvolume hebben opgelost
- Helpen kunstmatige slaapplaatsen vleermuizen? Experts zeggen dat er meer onderzoek nodig is
- Onderzoekers ontdekken hoe cellen decennia later infecties onthouden
- Welk proces treedt op wanneer het DNA van een gen een mRNA -molecuul maakt?
- Wordt een volledig chromosoom tijdens transcriptie tot een mRNA gemaakt?
- Stabiliserende zilverfilms voor zeer efficiënte brandstofcellen

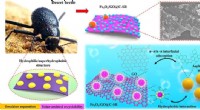
- Op woestijnkever geïnspireerde magnetische demulgator ontwikkeld met uitstekende olie-in-water-emulsiescheidingsprestaties
- Een manier bedenken om microplastics uit afvalwater te verwijderen - met okra, aloë

- Fluorescerende moleculen onthuld door kwantumchemie en machine learning

- Haaibestendig materiaal voor wetsuits kan levens helpen redden

 Op welke drie manieren lost de celdeling het groeiprobleem op?
Op welke drie manieren lost de celdeling het groeiprobleem op?  Dawn-missie naar asteroïdengordel komt ten einde
Dawn-missie naar asteroïdengordel komt ten einde Bepalen hoe vreemde oppervlakken en vloeistoffen op elkaar inwerken
Bepalen hoe vreemde oppervlakken en vloeistoffen op elkaar inwerken Verschillen plantencellen van dier door geen DNA te hebben?
Verschillen plantencellen van dier door geen DNA te hebben?  Pacific Islands Forum houdt virtuele klimaattop
Pacific Islands Forum houdt virtuele klimaattop Hoe wordt energie overgedragen wanneer het object in contact staat?
Hoe wordt energie overgedragen wanneer het object in contact staat?  Wat is de functie van een elektroscoop?
Wat is de functie van een elektroscoop?  Waarom is er minder zuurstof op de top van een berg?
Waarom is er minder zuurstof op de top van een berg?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

