
Wetenschap
Bereken de normaliteit van natriumhydroxide (NaOH) – een praktische gids
Bereken de normaliteit van natriumhydroxide (NaOH)
Auteur: Kittisak Kaewchalun / Getty Images
Normaliteit is een belangrijke maatstaf in de scheikunde die de concentratie van een oplossing uitdrukt in termen van gram-equivalenten per liter. Het is vooral waardevol voor het bereiden en hanteren van basisoplossingen zoals natriumhydroxide (NaOH), algemeen bekend als loog. Als u begrijpt hoe u de normaliteit kunt berekenen, zorgt u ervoor dat u veilig en nauwkeurig chemische oplossingen kunt formuleren voor industrieel, laboratorium- of huishoudelijk gebruik.
Wat is normaliteit?
Normaliteit (N) meet de hoeveelheid reactieve soorten in een oplossing. Het wordt gedefinieerd als:
N =gram opgeloste stof ÷ (liter oplossing × equivalent gewicht)
Het equivalentgewicht van een verbinding is de molaire massa gedeeld door het aantal equivalenten dat het kan doneren of accepteren in een reactie. Voor basen zoals NaOH is het aantal equivalenten gelijk aan het aantal hydroxide-ionen (OH⁻) dat het levert – één per molecuul.
Het equivalente gewicht van NaOH bepalen
Bereken eerst de molaire massa van NaOH:
- Na:22,989 g/mol
- O:15,999 g/mol
- H:1,008 g/mol
- Totaal: 39,996 g/mol
Omdat NaOH één OH⁻-ion per molecuul afgeeft, is het equivalentgewicht gelijk aan de molaire massa:39,996 g/equivalent.
Stapsgewijs voorbeeld
Stel dat je 12 gram NaOH oplost in 1 liter water. Met behulp van de normaliteitsformule:
N =12 g ÷ (1 L × 39,996 g/equiv)
Dit levert een normaliteit op van 0,30003 N, oftewel ongeveer 0,30 N.
Praktische tip: Controleer altijd nogmaals de molmassa's en zorg ervoor dat de volumemeting nauwkeurig is, aangezien kleine afwijkingen de normaliteit en de veiligheid van de oplossing kunnen beïnvloeden.
Waarom normaliteit ertoe doet
Nauwkeurige normaliteitsberekeningen zijn van cruciaal belang wanneer:
- Het formuleren van reinigingsmiddelen of industriële reagentia.
- Het uitvoeren van titraties of andere kwantitatieve analyses.
- Het garanderen van naleving van de veiligheidsrichtlijnen voor het hanteren van sterke bases.
Door de normaliteit onder de knie te krijgen, kunt u vol vertrouwen oplossingen voorbereiden die aan de vereiste specificaties voldoen en veilige laboratoriumpraktijken handhaven.
Illustratie: Pakin Songmor / Getty Images
 Wat zijn de term voornmaterialen met een zeer lage thermische energie en weerstand?
Wat zijn de term voornmaterialen met een zeer lage thermische energie en weerstand?  Beperkende reagentia begrijpen:productopbrengst bij chemische reacties berekenen
Beperkende reagentia begrijpen:productopbrengst bij chemische reacties berekenen  Onderzoekers laten zien dat materialen vanzelf sterker worden wanneer ze met zeer hoge snelheid worden geraakt
Onderzoekers laten zien dat materialen vanzelf sterker worden wanneer ze met zeer hoge snelheid worden geraakt Hoe de bewegingen van gasdeeltjes gerelateerd zijn aan druk door gas?
Hoe de bewegingen van gasdeeltjes gerelateerd zijn aan druk door gas?  Is zwavel een metalen niet -metaal of metalloïde?
Is zwavel een metalen niet -metaal of metalloïde?
 Waarom zou de persoon minder op de berg wegen dan de aardoppervlak?
Waarom zou de persoon minder op de berg wegen dan de aardoppervlak?  Op zoek naar superkoralen die aan de rand leven
Op zoek naar superkoralen die aan de rand leven Hoe het koopseizoen voor de feestdagen brandstof toevoegt aan een snel opwarmende planeet
Hoe het koopseizoen voor de feestdagen brandstof toevoegt aan een snel opwarmende planeet Eerste grote restauratieproject Carbon Landscape officieel geopend
Eerste grote restauratieproject Carbon Landscape officieel geopend Wat zijn enkele natuurvragen?
Wat zijn enkele natuurvragen?
Hoofdlijnen
- Wat zijn drie belangrijkste manieren waarop organismen op elkaar inwerken?
- Wat zijn conidiën?
- Wat hebben alle cellen?
- Wat is onderlinge afhankelijkheid van planten en mensen?
- Wat voor soort schimmels is de agaricus bisporus?
- Welke organismen bevatten celwanden met cellulose?
- Wat zijn tien van de meest dodelijkste bacterieën?
- Waarom wordt DNA als een polymeer beschouwd?
- Een andere massale verblekingsgebeurtenis verwoest het Great Barrier Reef. Wat is er nodig om koraal te laten overleven?
- Ultradunne roestlagen wekken elektriciteit op uit stromend water

- De juiste formule voor het opschalen van de productie van veelbelovend materiaal om water te decontamineren

- Nieuwe moleculen afgeleid van cannabidiol zijn ontworpen met krachtigere antioxidanten

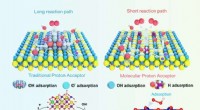
- Ontwerpstrategie op moleculair niveau kan de sleutel zijn tot het stimuleren van commerciële waterstofproductie
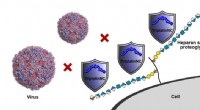
- Op metaal gebaseerde verbindingen maken de weg vrij voor nieuwe antivirale behandelingen
 Wat is de functie van osteogene cellen?
Wat is de functie van osteogene cellen?  Apple onthult premium iPhone XS, gezondheidsfuncties voor horloge (update)
Apple onthult premium iPhone XS, gezondheidsfuncties voor horloge (update) Ideeën voor een Shoebox Animal Habitat Project
Ideeën voor een Shoebox Animal Habitat Project  Does bacteria grow in cooked rice?
Does bacteria grow in cooked rice?  Vijf voorbeelden van een dier en zijn habitat?
Vijf voorbeelden van een dier en zijn habitat?  Verschil tussen windenergie en energie?
Verschil tussen windenergie en energie?  Kun je deze vergelijking Ba plus O2 in evenwicht brengen?
Kun je deze vergelijking Ba plus O2 in evenwicht brengen?  Vorming van de maan bracht water naar de aarde
Vorming van de maan bracht water naar de aarde
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

