
Wetenschap
Stikstofmonoxide (N₂O):structuur, eigenschappen en hechting
Structuur:
* Centraal atoom: Stikstof (N)
* Terminale atomen: Twee zuurstofatomen (O).
* Verbinding:
* Het centrale stikstofatoom is via een dubbele binding aan beide zuurstofatomen gebonden en een enkele binding .
* De zuurstofatomen zijn verbonden via een gecoördineerde covalente binding , waarbij een van de zuurstofatomen beide elektronen doneert om de binding te vormen.
Lewis-structuur:
```
O
||
N - N
||
O
```
Eigenschappen:
* Kleurloos gas: Bij kamertemperatuur is het een kleurloos gas met een licht zoete geur.
* Enigszins oplosbaar in water: Het lost in kleine mate op in water.
* Lachgas: Bekend om zijn verdovende en licht euforische effecten, daarom wordt het 'lachgas' genoemd.
* Oxidatiemiddel: Het kan bij bepaalde reacties als oxidatiemiddel werken.
* Gebruikt in de tandheelkunde: Lachgas wordt gebruikt als milde verdoving bij tandheelkundige ingrepen.
* Ander gebruik: Het wordt ook gebruikt als drijfgas in slagroomblikken, als additief in raketbrandstof en in de voedingsindustrie.
Covalente binding:
Distikstofmonoxide is een covalente verbinding omdat de stikstof- en zuurstofatomen elektronen delen om bindingen te vormen. Dit delen van elektronen resulteert in een stabielere rangschikking van atomen.
 Een vloeibaar mengsel van complexe koolwaterstofverbindingen wordt genoemd?
Een vloeibaar mengsel van complexe koolwaterstofverbindingen wordt genoemd?  Welke verbindingen zijn tetravalent?
Welke verbindingen zijn tetravalent?  Wat zijn de elementen aanwezig in Iron III Hydroxide?
Wat zijn de elementen aanwezig in Iron III Hydroxide?  Waarom zouden Hirsch en Buchner Funnels niet worden gebruikt voor de filtratie van hete oplossingen?
Waarom zouden Hirsch en Buchner Funnels niet worden gebruikt voor de filtratie van hete oplossingen?  Welk element wordt gebruikt om gevaarlijke straling te blokkeren?
Welk element wordt gebruikt om gevaarlijke straling te blokkeren?
 Blokkerig en rauw:maakt brutalistische architectuur een comeback?
Blokkerig en rauw:maakt brutalistische architectuur een comeback?  Aarde saai miljard jaar stilstaand, stinkende oceanen waren misschien nogal dynamisch
Aarde saai miljard jaar stilstaand, stinkende oceanen waren misschien nogal dynamisch Wat zijn de doelen en doelstellingen van een wetenschapsclub?
Wat zijn de doelen en doelstellingen van een wetenschapsclub?  Wat is op aarde de grootste bedreiging voor de biodiversiteit?
Wat is op aarde de grootste bedreiging voor de biodiversiteit?  Bestudeer gebieden met hoge concentraties in de Delaware Bay
Bestudeer gebieden met hoge concentraties in de Delaware Bay
Hoofdlijnen
- Hoe lichaamscellen zuurstof gebruiken om het leven kracht bij te zetten
- Waar wonen vroege organismen?
- Koala's hebben een vreemd dieet:zijn het bacteriën?
- Welk molecuul is verantwoordelijk voor het dragen van gentic informatie uit de kern van cel in cytoplasma?
- Welk type organismen zou geen cellulaire ademhaling uitvoeren?
- Onthulling van de moleculaire functies van lipidedruppeleiwitten in bladeren van Arabidopsis thaliana
- Wat is de wetenschapsapparaat?
- Doorbraak helpt verklaren hoe DNA in onze cellen is georganiseerd
- Horzels blijken de belangrijkste bestuivers te zijn van twee Angelica-soorten
- smartphone, blockchain-technologieën om nieuwe grenzen te openen in de strijd tegen voedselfraude

- Studie verandert lang gekoesterde concepten van celdecodering
- Nauwkeurige medicijndoseringen met protonvallen

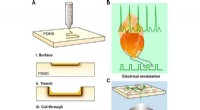
- Laserschrijven van met stikstof gedoteerd siliciumcarbide voor biologische modulatie
- Wanneer meer botvormende cellen gelijk zijn aan minder bot

 Wat verandert zetmeel in vóór de productie van de ademhalings -ATP?
Wat verandert zetmeel in vóór de productie van de ademhalings -ATP?  Ultradunne zonnecellen krijgen een boost:2D-perovskietverbinding heeft het juiste materiaal om omvangrijkere producten uit te dagen
Ultradunne zonnecellen krijgen een boost:2D-perovskietverbinding heeft het juiste materiaal om omvangrijkere producten uit te dagen  Lab ontwikkelt ongekend voorspellingsmodel voor natuurbranden op lange termijn
Lab ontwikkelt ongekend voorspellingsmodel voor natuurbranden op lange termijn De nadelen van staalconstructies
De nadelen van staalconstructies GRACE-satellieten van de volgende generatie arriveren op de lanceerplaats
GRACE-satellieten van de volgende generatie arriveren op de lanceerplaats Wat zijn de belangrijkste toepassingen van warmte-energie in de fysische wetenschap?
Wat zijn de belangrijkste toepassingen van warmte-energie in de fysische wetenschap?  Vleermuizen en insecten vechten in de tropen
Vleermuizen en insecten vechten in de tropen Microsoft-aandeelhouders verwerpen 2 activistische voorstellen
Microsoft-aandeelhouders verwerpen 2 activistische voorstellen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

