
Wetenschap
Koper (II) Sulfaat-uitdroging:de kleurverandering begrijpen
* Blauwe kleur: De blauwe kleur van koper(II)sulfaatpentahydraat komt van de watermoleculen die zijn gecoördineerd met het koper(II)-ion (Cu²⁺). Deze watermoleculen interageren met het koperion, beïnvloeden de elektronische structuur ervan en geven het een karakteristieke blauwe kleur.
* Verwarming en uitdroging: Wanneer je koper(II)sulfaat-pentahydraat verwarmt, worden de watermoleculen als stoom weggedreven. Dit proces wordt uitdroging genoemd.
* Kleurloos watervrij zout: Zodra het water is verwijderd, wordt het koper(II)-ion niet langer omringd door watermoleculen. Deze verandering in zijn omgeving verandert de elektronische structuur en resulteert in het verlies van zijn blauwe kleur. Het resulterende watervrije koper(II)sulfaat (CuSO₄) is een witte of lichtgrijze vaste stof.
De reactie kan als volgt worden samengevat:
CuSO₄•5H₂O (blauw) → CuSO₄ (wit/lichtgrijs) + 5H₂O (g)
Samenvattend komt de blauwe kleur van koper(II)sulfaatpentahydraat voort uit de interactie tussen het koper(II)-ion en watermoleculen. Bij verhitting worden de watermoleculen verwijderd, waardoor de omgeving van het koperion verandert en zijn blauwe kleur verliest.
Hoofdlijnen
- Hoe beïnvloedt de omgeving de migratie van een organisme?
- Nieuwe studie laat zien hoe mierenkolonies zich anders gedragen in verschillende omgevingen
- Mojave-woestijnschildpad wordt officieel toegevoegd aan de bedreigde lijst van Californië
- Waarom hebben wetenschappers genetische modificatie toegepast op groenten en fruit?
- Die eenzame, steile gomboom op een boerderij? Het is een reddingslijn voor koala's
- Hoe katten en honden verwerkingsparabenen consumeren
- Waarom zijn wetenschappers geïnteresseerd in stamcelonderzoek?
- Wat is een andere naam voor heterozygoot?
- Wat was het algemene doel van Human Genome Project?
- Massaspectrometrietechniek helpt bij het identificeren van vervalste manuscripten van Robert Burns

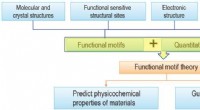
- De cruciale rol van functionele motieven—microstructurele eenheden die materiële functies bepalen—in materiaalonderzoek
- Bacteriën produceren goud door giftige metalen te verteren

- Een efficiëntere, veiliger alternatief voor het inkopen van koper via bacteriën

- Ingenieurs introduceren een nieuwe aanpak voor het recyclen van kunststoffen

 Is vloeibaar gas waterdamp ja of nee?
Is vloeibaar gas waterdamp ja of nee?  Waarschuwingsborden voor een Hurricane
Waarschuwingsborden voor een Hurricane Landvormen van Connecticut
Landvormen van Connecticut  Is MgSO4 · 7H2O zuur in oplossing?
Is MgSO4 · 7H2O zuur in oplossing?  Welke golflengten dragen de meeste energie?
Welke golflengten dragen de meeste energie?  Wat zijn de twee soorten condensatie?
Wat zijn de twee soorten condensatie?  Hoeveel mol chloorgas zit er in 9,02 x 1023 atomen?
Hoeveel mol chloorgas zit er in 9,02 x 1023 atomen?  Kun je enkele voorbeelden geven van geothermische energie?
Kun je enkele voorbeelden geven van geothermische energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


