
Wetenschap
Zilverchloride (AgCl) in water:oplosbaarheid en reactie
Hier is een overzicht van de reactie in water:
* Ontbinding:
* Een kleine hoeveelheid AgCl lost op in water en vormt zilverionen (Ag+) en chloride-ionen (Cl-):
* AgCl(s) ⇌ Ag+(aq) + Cl-(aq)
* Evenwicht:
* Deze reactie is een evenwichtsreactie, wat betekent dat deze in beide richtingen verloopt.
* Het oplossingsproces wordt beperkt door de productconstante met lage oplosbaarheid (Ksp) van AgCl, dat is 1,8 × 10⁻¹⁰ bij 25°C. Dit betekent dat het product van de concentraties Ag+ en Cl-ionen in oplossing erg klein is, wat erop wijst dat er heel weinig AgCl oplost.
* Neerslag:
* Als de concentratie van Ag+ of Cl-ionen in de oplossing wordt verhoogd (bijvoorbeeld door meer AgNO3 of NaCl toe te voegen), verschuift het evenwicht naar links, wat leidt tot precipitatie van meer AgCl uit de oplossing.
Factoren die de oplosbaarheid van AgCl beïnvloeden:
* Temperatuur: De oplosbaarheid neemt enigszins toe met de temperatuur.
* Gemeenschappelijk ioneffect: De aanwezigheid van andere Ag+ of Cl-ionen in de oplossing zal de oplosbaarheid van AgCl verminderen vanwege het principe van Le Chatelier.
* Complexe vorming: De aanwezigheid van liganden die complexen kunnen vormen met zilverionen (bijvoorbeeld ammoniak, cyanide) kan de oplosbaarheid van AgCl vergroten.
Over het geheel genomen is de reactie van zilverchloride in water een beperkt oplossingsproces, waarbij het grootste deel van AgCl achterblijft als een vast neerslag.
 Het verminderen van vervuiling door nutriënten helpt koraal bleken te weerstaan
Het verminderen van vervuiling door nutriënten helpt koraal bleken te weerstaan In termen van de geografische themalocatie versus plaats, verschilt de plaats van in die zin dat het zich meer op richt op?
In termen van de geografische themalocatie versus plaats, verschilt de plaats van in die zin dat het zich meer op richt op?  Terug naar het wild:hoe ‘ungardening’ wortel schoot in Amerika
Terug naar het wild:hoe ‘ungardening’ wortel schoot in Amerika  Uit eten, inademen
Uit eten, inademen Convergente oplichters:hoe kortschildkevers blijven evolueren tot legermierenparasieten
Convergente oplichters:hoe kortschildkevers blijven evolueren tot legermierenparasieten
Hoofdlijnen
- Hoeveel cellen zijn nodig om een nieuw organisme te maken in eencellige organismen?
- Een cel die niet in homeostase is, zou?
- De sleutel tot het kweken van natuurlijk weefsel voor de reconstructie van het vrouwelijk voortplantingssysteem ontgrendeld
- Hoeveel verschillende soorten eiwitten bevat één cel?
- Hoe krijgen mensen stikstof in hun lichaam?
- Wat bevatten groene organellen in plantencellen die voedsel maken?
- Wat zijn de twee hoofdfasen van celdeling?
- Welke velden van moderne microbiologie houdt zich niet direct bezig met de genetische kenmerken van een cel?
- Welke twee lichaamssystemen zijn betrokken bij de regulatie?
- Chemici rapporteren een gedetailleerde beschrijving van azopyrazolonkleurstoffen

- Studie van olifant, capibara, mensenhaar vindt dat dikker haar niet altijd sterker is

- Polystyreen versus polyurethaan:belangrijkste verschillen in samenstelling, thermische en chemische prestaties

- Nieuw goedkoop materiaal voor verlichting en diagnostiek produceert wit licht dat zonlicht imiteert

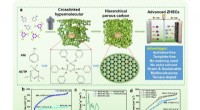
- Meervoudig gedoteerde hiërarchische poreuze koolstoffen voor superieure opslag van zinkionen
 Een dubbele breker 20 ampère en 30 ampère?
Een dubbele breker 20 ampère en 30 ampère?  Amerikaanse gigant IFF koopt Israels Frutarom voor 7 miljard dollar
Amerikaanse gigant IFF koopt Israels Frutarom voor 7 miljard dollar Zijn hyolieten paleozoïsche lophophorates?
Zijn hyolieten paleozoïsche lophophorates? Wat zijn de drie druk die leiden tot biodiversiteit volgens de theorie van eilandbiogeografie?
Wat zijn de drie druk die leiden tot biodiversiteit volgens de theorie van eilandbiogeografie?  Hoe mummies werken
Hoe mummies werken  Afbeelding:menselijke endotheelcel in de ruimte
Afbeelding:menselijke endotheelcel in de ruimte Hoeveel mol ammoniakgas wordt gevonden in een container van 202 ml bij 35C en 750 mmHg?
Hoeveel mol ammoniakgas wordt gevonden in een container van 202 ml bij 35C en 750 mmHg?  Hoe snel is de snelheid van het licht?
Hoe snel is de snelheid van het licht?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

