
Wetenschap
Stikstof versus zuurstof:bindingsreactiviteit begrijpen
1. Elektronische configuratie:
* Stikstof (N): Heeft een elektronische configuratie van 2s² 2p³, met drie ongepaarde elektronen in zijn p-orbitalen.
* Zuurstof (O): Heeft een elektronische configuratie van 2s² 2p⁴, met twee ongepaarde elektronen in zijn p-orbitalen.
De halfgevulde p-orbitalen van stikstof zorgen voor extra stabiliteit, waardoor het minder waarschijnlijk is dat er elektronen worden gewonnen of verloren. Zuurstof, met zijn twee ongepaarde elektronen, wil graag bindingen vormen om een stabiele octetconfiguratie te bereiken.
2. Hechtsterkte:
* Stikstof (N₂): Vormt een drievoudige binding tussen twee stikstofatomen. Deze drievoudige binding is extreem sterk en vereist een grote hoeveelheid energie om te breken.
* Zuurstof (O₂): Vormt een dubbele binding tussen twee zuurstofatomen. Deze dubbele binding is sterk maar zwakker dan de drievoudige binding in stikstof.
De sterkere drievoudige binding in stikstof maakt het veel moeilijker om te breken en te reageren met andere elementen.
3. Kleiner formaat:
* Stikstof: Heeft een kleinere atoomstraal dan zuurstof.
* Zuurstof: Heeft een grotere atoomstraal dan stikstof.
De kleinere omvang van stikstof leidt tot een hogere elektronendichtheid en sterkere aantrekkingskracht tussen de stikstofatomen in het N₂-molecuul, wat verder bijdraagt aan de lagere reactiviteit ervan.
4. Elektronegativiteit:
* Stikstof: Heeft een hogere elektronegativiteit dan zuurstof.
Dit betekent dat het waarschijnlijker is dat stikstofatomen elektronen in een binding aantrekken, waardoor het minder waarschijnlijk is dat ze elektronen verliezen en reageren.
Samengevat: De stabiele elektronische configuratie van stikstof, de sterke drievoudige binding, het kleinere formaat en de hogere elektronegativiteit dragen allemaal bij aan de lagere reactiviteit ervan in vergelijking met zuurstof. Dit maakt stikstof onder normale omstandigheden een inert gas, terwijl zuurstof gemakkelijk deelneemt aan chemische reacties.
 Hoe A.I. veroverde een vulkanen veranderend lavameer
Hoe A.I. veroverde een vulkanen veranderend lavameer Zuid-Afrika om kolengestookte energie te verhogen, klimaatverontwaardiging aanwakkeren
Zuid-Afrika om kolengestookte energie te verhogen, klimaatverontwaardiging aanwakkeren Groeisnelheid van de Royal Poinciana
Groeisnelheid van de Royal Poinciana  Wat is de menselijke impact van een gematigd regenwoud Biome?
Wat is de menselijke impact van een gematigd regenwoud Biome?  Beschrijf 2 voorwaarden op aarde die de planeet gunstig maken voor het leven?
Beschrijf 2 voorwaarden op aarde die de planeet gunstig maken voor het leven?
Hoofdlijnen
- Is het levend of dood? Team laat zien hoe je de thermische handtekeningen van afzonderlijke cellen kunt meten
- Wat is celcompartimentering en waarom gebeurt het?
- Wat is gebruik van micro -organismen in biotechnologie?
- Wat zijn de twee belangrijkste doelen van mitose?
- Wat zijn 3 dingen die meiose en mitose gemeen hebben?
- Welke processen worden het meest geholpen door de aanwezigheid van bacteriën in het menselijk lichaam?
- Neteldieren controleren bacteriën op afstand
- Welk enzym verbindt nucleotiden met elkaar tijdens DNA -replicatie?
- Hoe zijn meercellige organismen efficiënter dan eencellige organismen?
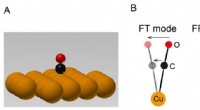
- Opheldering van trillingsenergie van een enkel molecuul in een extern krachtveld
- Nieuwe inkjetprintmethode kan het ontdekken van medicijnen en geprinte gepersonaliseerde medicijnafgifte versnellen

- Video — Wijnsnobisme:feit versus fictie

- Een vereenvoudigd nieuw proces zet houtafval uit landbouw en bosbeheer om in ethanol

- Populair nieuw bouwmateriaal helpt bij het meten van eiwitdeeltjes
 Hoe het Amazon-wederverkopersleger van Miami consumenten over de hele wereld bedient – en miljoenen verdient
Hoe het Amazon-wederverkopersleger van Miami consumenten over de hele wereld bedient – en miljoenen verdient  Maakt het eten van bamboe het moeilijker voor panda’s om zich voort te planten?
Maakt het eten van bamboe het moeilijker voor panda’s om zich voort te planten?  Hoe uraniumwinning werkt
Hoe uraniumwinning werkt  Te midden van droogte, Colorado-spanten trekken naar oases terwijl ze kunnen
Te midden van droogte, Colorado-spanten trekken naar oases terwijl ze kunnen Hoeveel onbeschadigde regenwoudvalleien zijn er vandaag nog over aan de regenkust van BC?
Hoeveel onbeschadigde regenwoudvalleien zijn er vandaag nog over aan de regenkust van BC?  Ardern toert verwoestende overstromingen in Nieuw-Zeeland
Ardern toert verwoestende overstromingen in Nieuw-Zeeland Facebook kan studenten met minder zelfvertrouwen helpen om relaties op te bouwen
Facebook kan studenten met minder zelfvertrouwen helpen om relaties op te bouwen Ruimtevaartuig stuurt laatste stukje gegevens terug van Pluto-flyby 2015
Ruimtevaartuig stuurt laatste stukje gegevens terug van Pluto-flyby 2015
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

