
Wetenschap
Waterstof in het periodiek systeem:zijn unieke positie begrijpen
* Groep 1 (Alkalimetalen): Waterstof heeft één valentie-elektron, net als de alkalimetalen. Dit betekent dat het één elektron kan verliezen om een positief ion (H+) te vormen. Het kan reageren met niet-metalen om verbindingen te vormen, vergelijkbaar met alkalimetalen die reageren met niet-metalen.
* Groep 17 (Halogenen): Waterstof kan een elektron verkrijgen om een negatief ion (H-) te vormen, vergelijkbaar met hoe halogenen een elektron verkrijgen om negatieve ionen te vormen. Het kan ook diatomische moleculen (H2) vormen, vergelijkbaar met halogenen zoals chloor (Cl2).
De unieke positie van waterstof:
* Vanwege zijn unieke eigenschappen wordt waterstof soms afzonderlijk van beide groepen boven het periodiek systeem geplaatst. Dit benadrukt de unieke kenmerken ervan.
* Sommige periodieke tabellen plaatsen waterstof bovenaan zowel Groep 1 als Groep 17, en erkennen het dubbele karakter ervan.
Samengevat:
De positie van waterstof op het periodiek systeem weerspiegelt zijn vermogen om zich zowel als een alkalimetaal als als een halogeen te gedragen. Het is uniek in zijn reactiviteit en chemische eigenschappen, wat de speciale plaatsing ervan rechtvaardigt.
Hoofdlijnen
- Wat is een verschil tussen het dier- en plantencel?
- Reproductie in bryophyllum vindt plaats in?
- Wat zijn de Charcteristics of Ambahan?
- Wat zijn alle organellen in dierencellen en hun functies?
- Op welke agar groeit Corynebacterium xerose?
- Waarom zijn planten nodig voor het overleven van alle dieren op aarde en waarom?
- Tot de kern komen van hoe cowpea groeit in moeilijke omstandigheden
- Welke vier stikstofbases zijn purines?
- Wat is de belangrijkste bijdrage aan de biologie?
- Wetenschappers optimaliseren de productiviteit van het productieproces van pultrusie

- Roestvorming begrijpen:chemie, oorzaken en preventie

- De structuur van de mysterieuze blauwe wervelende vlam onthullen

- Nieuw thermodynamisch raamwerk voor cellen
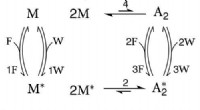
- Vorming van goudbindingen in realtime gevolgd met behulp van nieuwe moleculaire spectroscopietechniek

 Wat zijn de 10 wetenschapstakken die hun betekenissen geven?
Wat zijn de 10 wetenschapstakken die hun betekenissen geven?  Wat is de naam Worm die papier eet?
Wat is de naam Worm die papier eet?  Hoe een Punnett-plein te doen
Hoe een Punnett-plein te doen  Welke toestand van materie in welke watermoleculen het snelst bewegen?
Welke toestand van materie in welke watermoleculen het snelst bewegen?  Welke twee krachten moeten even sterk zijn om een dalende object terminale snelheid te bereiken?
Welke twee krachten moeten even sterk zijn om een dalende object terminale snelheid te bereiken?  Klein knaagdier, grote eetlust:onderzoekers identificeren de voedingseffecten van invasieve muizen op de Farallon-eilanden
Klein knaagdier, grote eetlust:onderzoekers identificeren de voedingseffecten van invasieve muizen op de Farallon-eilanden Is een maanverduistering een goed gemiseerde maanfase?
Is een maanverduistering een goed gemiseerde maanfase?  Hiaten in het opruimen van meth-labs
Hiaten in het opruimen van meth-labs
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


