
Wetenschap
Ionisatie-energie en atomaire stabiliteit:een omgekeerd evenredige relatie
Hier is een overzicht:
* Ionisatie-energie is de minimale energie die nodig is om een elektron te verwijderen uit een gasvormig atoom in zijn elektronische grondtoestand.
* Stabiliteit verwijst naar de neiging van een atoom om weerstand te bieden aan veranderingen, zoals het verliezen van elektronen.
Hogere ionisatie-energie betekent een stabieler atoom:
*Als een atoom een hoge ionisatie-energie heeft, betekent dit dat er veel energie nodig is om een elektron te verwijderen. Dit suggereert dat de elektronen stevig aan de kern zijn gebonden, waardoor het atoom minder snel een elektron verliest en daardoor stabieler is.
Een lagere ionisatie-energie betekent een minder stabiel atoom:
* Omgekeerd geeft een lage ionisatie-energie aan dat een elektron gemakkelijk kan worden verwijderd. Dit impliceert dat de elektronen zwak gebonden zijn aan de kern, waardoor het atoom waarschijnlijker een elektron verliest en dus minder stabiel is.
Belangrijke factoren die de ionisatie-energie beïnvloeden:
* Nucleaire lading: Een hogere nucleaire lading (meer protonen) leidt tot een sterkere aantrekkingskracht tussen de kern en elektronen, wat resulteert in hogere ionisatie-energie en grotere stabiliteit.
* Atomische grootte: Kleinere atomen hebben elektronen dichter bij de kern, ervaren een sterkere aantrekkingskracht en hebben daarom een hogere ionisatie-energie en een grotere stabiliteit.
* Elektronenafscherming: Elektronen in de binnenste schillen beschermen de buitenste elektronen tegen de volledige nucleaire lading, waardoor de aantrekkingskracht wordt verminderd en de ionisatie-energie wordt verlaagd, waardoor het atoom minder stabiel wordt.
* Elektronenconfiguratie: Halfgevulde en volledig gevulde subshells zijn stabieler dan gedeeltelijk gevulde subshells. Dit beïnvloedt de ionisatie-energie en dus de stabiliteit.
Voorbeeld:
* Edelgassen hebben zeer hoge ionisatie-energieën vanwege hun volledige buitenste elektronenschillen, waardoor ze extreem stabiel zijn.
* Alkalimetalen hebben zeer lage ionisatie-energieën omdat ze slechts één elektron in hun buitenste schil hebben, waardoor ze gemakkelijk geïoniseerd en minder stabiel zijn.
Samengevat: Hoge ionisatie-energie impliceert een sterke aantrekking van de elektronenkern, wat leidt tot grotere stabiliteit. Omgekeerd impliceert een lage ionisatie-energie een zwakke aantrekking van de elektronkern, wat resulteert in een lagere stabiliteit.
 Welk molecuul reageert met pyruvinezuur om CO2 af te geven?
Welk molecuul reageert met pyruvinezuur om CO2 af te geven?  Wat zijn de tools die wetenschappers gebruikten om atomen te observeren?
Wat zijn de tools die wetenschappers gebruikten om atomen te observeren?  Tijdens het uitvoeren van een experiment ontdek je een bepaalde stof die uit cel gaat door diffusie wat zou kunnen concluderen over de concentratie deze stof?
Tijdens het uitvoeren van een experiment ontdek je een bepaalde stof die uit cel gaat door diffusie wat zou kunnen concluderen over de concentratie deze stof?  Waarom zout toevoegen aan water Maak het kouder?
Waarom zout toevoegen aan water Maak het kouder?  Kan zilver zink uit zijn zoutoplossing verdringen?
Kan zilver zink uit zijn zoutoplossing verdringen?
 Beschrijf drie plaatsen die koolstof bestaat in het milieu buiten de leefomgeving?
Beschrijf drie plaatsen die koolstof bestaat in het milieu buiten de leefomgeving?  Hoe de klimaatoorlogen te winnen - praat over lokale vervuiling, niet over het broeikaseffect
Hoe de klimaatoorlogen te winnen - praat over lokale vervuiling, niet over het broeikaseffect Wetenschappers lossen puzzel over luchtkwaliteit op:waarom blijft ozon lang hangen na het verbod?
Wetenschappers lossen puzzel over luchtkwaliteit op:waarom blijft ozon lang hangen na het verbod? Oorlog verklaard aan de groeiende e-waste-crisis ter wereld
Oorlog verklaard aan de groeiende e-waste-crisis ter wereld NASA vindt tropische depressie 23Ws sterkste stormen in twee landen
NASA vindt tropische depressie 23Ws sterkste stormen in twee landen
Hoofdlijnen
- Wat is polyprotisch zuur?
- RNA -polymerase beweegt in welke richting langs het DNA?
- Kun jij de vier belangrijkste biomen van BC noemen?
- Waar in de natuur zijn enzymen gevonden?
- Wat zijn enkele kenmerken of moerassen?
- Wat is de naam van het project dat genen heeft gesequenced?
- Welke organen zijn gemaakt van bindweefsel?
- CDC geeft dringende waarschuwing over toenemende gevallen van de ziekte van Chagas die verband houden met "Kissing Bug"
- Rubisco:het meest overvloedige eiwit op aarde en zijn rol in de fotosynthese
- Move over Rover:er is een nieuwe snuffelende krachtpatser in de buurt

- Video:Hoe airbags werken

- Robijnen op saffier:recept voor het maken van kristallen in flux
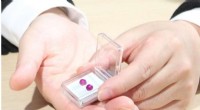
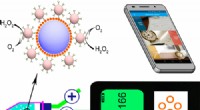
- Nieuwe sensoren kunnen een meer betaalbare detectie van vervuiling en ziekten mogelijk maken
- Pneumatische dubbelwerkende cilinders:toepassingen in de industrie, robotica en daarbuiten

 Welke wet relateert druk en temperatuur bij een constant volume naarmate toeneemt toeneemt?
Welke wet relateert druk en temperatuur bij een constant volume naarmate toeneemt toeneemt?  Koolstofopname in hergroeiend Amazonewoud bedreigd door klimaat en menselijke verstoring
Koolstofopname in hergroeiend Amazonewoud bedreigd door klimaat en menselijke verstoring Energie wordt geproduceerd door de trillingen van elektrisch geladen deeltjes?
Energie wordt geproduceerd door de trillingen van elektrisch geladen deeltjes?  Wat zijn de 2 meest voorkomende elementen en verbindingen?
Wat zijn de 2 meest voorkomende elementen en verbindingen?  Hoe de schokveer te bepalen
Hoe de schokveer te bepalen  Hoe is chemie gerelateerd aan alchemie?
Hoe is chemie gerelateerd aan alchemie?  Waarom ondersteunen de lichaamsstructuren van sommige soorten de theorieën?
Waarom ondersteunen de lichaamsstructuren van sommige soorten de theorieën?  GraphExeter-materiaal verlicht een heldere nieuwe toekomst voor flexibele verlichtingsapparaten
GraphExeter-materiaal verlicht een heldere nieuwe toekomst voor flexibele verlichtingsapparaten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

