
Wetenschap
Berekening van beperkende reagentia:natriumcarbonaat en calciumchloride
1. Schrijf de gebalanceerde chemische vergelijking:
Na₂CO₃(aq) + CaCl₂•2H₂O(aq) → CaCO₃(s) + 2NaCl(aq) + 2H₂O(l)
2. Bereken de molmassa's:
* Na₂CO₃:(2 * 22,99) + 12,01 + (3 * 16,00) =105,99 g/mol
* CaCl₂•2H₂O:40,08 + (2 * 35,45) + (2 * 18,02) =147,02 g/mol
3. Massa omrekenen naar mol:
* Mol Na₂CO₃:1,00 g / 105,99 g/mol =0,00943 mol
* Mol CaCl₂•2H₂O:1,00 g / 147,02 g/mol =0,00680 mol
4. Bepaal de beperkende reactant:
* Gebruik de molverhouding uit de gebalanceerde vergelijking: Uit de vergelijking blijkt een molverhouding van 1:1 tussen Na₂CO3 en CaCl₂·2H₂O.
* Vergelijk moedervlekken: Omdat we minder mol CaCl₂•2H₂O (0,00680 mol) hebben dan Na₂CO₃ (0,00943 mol), CaCl₂•2H₂O is de beperkende reactant.
Uitleg:
De beperkende reactant is degene die als eerste volledig wordt verbruikt, waardoor de reactie niet verder kan verlopen. In dit geval stopt de reactie, ook al hebben we meer mol Na₂CO₃, wanneer alle CaCl₂·2H₂O is opgebruikt.
 Klimaatverandering intensiveert droogtes in Europa
Klimaatverandering intensiveert droogtes in Europa Identificeer drie manieren waarop de wetenschap uw leven beïnvloedt?
Identificeer drie manieren waarop de wetenschap uw leven beïnvloedt?  Landbouw voor natuurlijke winst in China
Landbouw voor natuurlijke winst in China Grootte van bosbrand in Oregon onderstreept uitgestrektheid van het westen van de VS
Grootte van bosbrand in Oregon onderstreept uitgestrektheid van het westen van de VS Hoeveel veranderingen in de plantengemeenschap beïnvloeden andere eigenschappen van het ecosysteem?
Hoeveel veranderingen in de plantengemeenschap beïnvloeden andere eigenschappen van het ecosysteem?
Hoofdlijnen
- Wat is de genetische definitie van evolutie?
- Onderzoek bij vleermuizen en knaagdieren biedt inzicht in de manier waarop virussen zich over soorten verspreiden
- Welk plantenweefsel transporteert suikeroplossing?
- Wat wordt gesynthetiseerd door RNA -polymerase?
- Een functie van homeotische genen is?
- De hersenschors heeft een naam die letterlijk betekent dat het de schors is van welk orgel?
- Wat is een evolutionair nummer?
- Wat is de Outerlayer voor een boom?
- Wat is de studie van alle levensvormen?
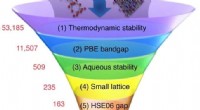
- Uitgebreide elektronische structuurmethoden voor materiaalontwerp
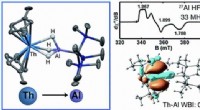
- Thorium-aluminiumcomplex het eerste met een actinide-element dat elektronen afstaat bij binding met een metaal
- Polymerisatieproces van hydrogelmicrosferen op video

- Moderne alchemie creëert lichtgevende ijzermoleculen
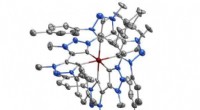
- Onderzoekers ontwikkelen krachtige strategie voor het maken van nieuwe natuurlijke enzymen

 Wat is de naam van verbinding gemaakt met natrium en broom?
Wat is de naam van verbinding gemaakt met natrium en broom?  Geometrisch verbijsterende quasikristallen gevonden in het puin van de allereerste nucleaire explosie
Geometrisch verbijsterende quasikristallen gevonden in het puin van de allereerste nucleaire explosie Stuctuur van een celmembraan
Stuctuur van een celmembraan Wat duwt voedsel door het spijsverteringskanaal?
Wat duwt voedsel door het spijsverteringskanaal?  Hoe Wendigoe's werken
Hoe Wendigoe's werken  Hoe helpt de wetenschappelijke methode wetenschapper?
Hoe helpt de wetenschappelijke methode wetenschapper?  Google voert inspanningen op om nieuwsorganisaties te helpen, met $300 mn
Google voert inspanningen op om nieuwsorganisaties te helpen, met $300 mn Onderzoekers ontwikkelen eerste model om grootschalige productie van ultradun grafeen te begeleiden
Onderzoekers ontwikkelen eerste model om grootschalige productie van ultradun grafeen te begeleiden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

