
Wetenschap
Azijnzuur en natriumacetaat als bufferoplossing:chemie uitgelegd
Hoe het werkt:
* Azijnzuur (CH3COOH) is een zwak zuur. Het ioniseert slechts gedeeltelijk in water, wat betekent dat het niet alle waterstofionen (H+) gemakkelijk afstaat.
* Natriumacetaat (CH3COONa) is het zout van azijnzuur. Het dissocieert volledig in water en levert acetaationen (CH3COO-).
Bufferactie:
1. Weerstand tegen pH-veranderingen door toegevoegd zuur: Als je een sterk zuur (zoals HCl) aan de buffer toevoegt, reageren de acetaationen (CH3COO-) uit het natriumacetaat met de toegevoegde H+-ionen om azijnzuur (CH3COOH) te vormen. Deze reactie verbruikt de toegevoegde H+, waardoor een significante daling van de pH wordt voorkomen.
CH3COO- + H+ ⇌ CH3COOH
2. Weerstand bieden aan pH-veranderingen door toegevoegde base: Als je een sterke base (zoals NaOH) aan de buffer toevoegt, reageert het azijnzuur (CH3COOH) met de toegevoegde OH-ionen om acetaationen (CH3COO-) en water (H2O) te vormen. Deze reactie verbruikt de toegevoegde OH-, waardoor een significante stijging van de pH wordt voorkomen.
CH3COOH + OH- ⇌ CH3COO- + H2O
Belangrijkste punten:
* Buffercapaciteit: De buffer is bestand tegen pH-veranderingen binnen een bepaald bereik, bepaald door de concentraties van het zwakke zuur en zijn geconjugeerde base (in dit geval acetaationen).
* pH van de buffer: De pH van de bufferoplossing kan worden berekend met behulp van de Henderson-Hasselbalch-vergelijking, waarbij rekening wordt gehouden met de pKa van het zwakke zuur en de verhouding van de concentraties van het zuur en zijn geconjugeerde base.
Samengevat:
Het azijnzuur/natriumacetaatbuffersysteem is effectief bestand tegen veranderingen in de pH door te reageren met toegevoegde zuren of basen, waardoor een relatief stabiele pH binnen een specifiek bereik wordt gehandhaafd. Dit maakt het nuttig in toepassingen waarbij pH-controle van cruciaal belang is, zoals in biologische systemen of chemische reacties.
 Wat zijn Brisling Sardines?
Wat zijn Brisling Sardines?  Hoe definieer je een natuurlijke satelliet?
Hoe definieer je een natuurlijke satelliet?  Onderzoek brengt microplastics in verband met menselijke gezondheidsproblemen, maar er is nog veel dat we niet weten
Onderzoek brengt microplastics in verband met menselijke gezondheidsproblemen, maar er is nog veel dat we niet weten  Nieuwe Jurassic Dinosaur Discovery onthult 150 miljoen jaar oude evolutionaire puzzel
Nieuwe Jurassic Dinosaur Discovery onthult 150 miljoen jaar oude evolutionaire puzzel  IJzerchemie is van belang voor de opname van koolstof in de oceaan
IJzerchemie is van belang voor de opname van koolstof in de oceaan
Hoofdlijnen
- Wat draagt voedsel en water naar de cellen in een blad?
- Is er zoiets als een vrouwelijke cel en mannelijke cel?
- Hoe je een vink kunt laten uitsterven
- Waarom beginnen cellen een andere cel oncontroleerbaar te reproduceren en een tumor te produceren?
- Een middel om vrij grote deeltjes in de cel te brengen?
- Wat zijn de twee factoren die de efficiëntie van een enzym beïnvloeden?
- Het belangrijkste orgaan in ons lichaam zijn de hersenen?
- Hoe behoudt de afwisseling van meiose en bemesting in levenscycli die seksueel reproducerende organismen voor elke soort normaal chromosoomtelling behouden?
- Waarom stoppen mensen dingen in categorieën?
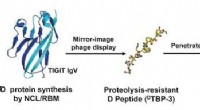
- Checkpointblokkade door een D-peptide voor kankerimmunotherapie
- Onderzoekers ontdekken nieuwe moleculen voor het volgen van de ziekte van Parkinson
- Nieuwe katalysebenadering reduceert koolstofdioxide tot methaan

- Directe waarneming van de ad- en desorptie van gastatomen in een mesoporeuze gastheer

- Electrospun vezels weven nieuwe medische innovaties

 Welke energie gebruikt tv?
Welke energie gebruikt tv?  Wat is waar aan de totale mechanische energie van een slinger bij afwezigheid van wrijving?
Wat is waar aan de totale mechanische energie van een slinger bij afwezigheid van wrijving?  AI-analyse van satellietbeelden laat zien dat de ineenstorting van de Sovjet-Unie in de jaren negentig de uitstoot van methaan verhoogde, ondanks de lagere olie- en gasproductie
AI-analyse van satellietbeelden laat zien dat de ineenstorting van de Sovjet-Unie in de jaren negentig de uitstoot van methaan verhoogde, ondanks de lagere olie- en gasproductie  In welke vorm verkrijgen de meeste organismen stikstof?
In welke vorm verkrijgen de meeste organismen stikstof?  Is een Dall Sheep Herbivore Carnivore of Omnivore waarom?
Is een Dall Sheep Herbivore Carnivore of Omnivore waarom?  NASA stelt een magnetisch schild voor om de atmosfeer van Mars te beschermen
NASA stelt een magnetisch schild voor om de atmosfeer van Mars te beschermen Leisteen en marmer zijn voorbeelden van wat voor soort rockfamilie?
Leisteen en marmer zijn voorbeelden van wat voor soort rockfamilie?  Hoop voor salamanders? Studie herkalibreert de effecten van klimaatverandering
Hoop voor salamanders? Studie herkalibreert de effecten van klimaatverandering
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

