
Wetenschap
Ferro versus non-ferro metaalcorrosie:de verschillen begrijpen
Corrosie van ferro- versus non-ferrometalen:een analyse
Hoewel zowel ferro- als non-ferrometalen kunnen corroderen, verschillen de mechanismen en producten van corrosie aanzienlijk. Hier is een overzicht:
Ferrometalen (op ijzerbasis)
* Mechanisme: Voornamelijk elektrochemische corrosie . Dit omvat de vorming van een elektrochemische cel waarin ijzer als anode fungeert, elektronen verliest en oxideert om ijzerionen te vormen (Fe²⁺). De elektronen stromen naar de kathode, meestal een minder edel metaal of een ander deel van het ijzeroppervlak, waar ze zuurstof uit de omgeving verminderen om hydroxide-ionen (OH⁻) te vormen. Deze ionen reageren vervolgens met ijzerionen en vormen roest (Fe₂O₃·xH₂O), een gehydrateerd ijzeroxide.
* Producten: Roest, een roodbruin, schilferig oxide dat poreus is en verdere corrosie mogelijk maakt.
* Factoren die corrosie beïnvloeden:
* Aanwezigheid van vocht: Voor roestvorming zijn water en zuurstof nodig.
* Elektrolyt: De aanwezigheid van zouten, zuren of andere elektrolyten versnelt het elektrochemische proces.
* Spanning: Mechanische spanning kan de corrosiesnelheid verhogen.
* Temperatuur: Hogere temperaturen verhogen doorgaans de corrosiesnelheid.
* pH: De pH van de omgeving kan de snelheid en het type corrosie beïnvloeden.
* Bescherming:
* Coatings: Verf, email en galvanisatie (coating met zink) kunnen voorkomen dat vocht en zuurstof het metalen oppervlak bereiken.
* Legering: Door elementen als chroom, nikkel en molybdeen aan ijzer toe te voegen, kunnen corrosiebestendige roestvaste staalsoorten ontstaan.
* Kathodische bescherming: Een actiever metaal gebruiken (bijvoorbeeld zink) om zichzelf op te offeren en het ferrometaal te beschermen.
Non-ferrometalen
* Mechanisme: Varieert afhankelijk van het specifieke metaal. Enkele veel voorkomende typen zijn:
* Oxidatie: Vorming van oxiden op het metaaloppervlak (bijvoorbeeld aluminiumoxide).
* Zwaveling: Reactie met zwavelverbindingen om sulfiden te vormen (bijvoorbeeld kopersulfide).
* Chlorering: Reactie met chloorverbindingen om chloriden te vormen (bijvoorbeeld zilverchloride).
* Producten: Varieert afhankelijk van het metaal- en corrosieproces.
* Factoren die corrosie beïnvloeden:
* Omgeving: De aanwezigheid van specifieke elementen zoals zwavel, chloor of zuurstof kan corrosie versnellen.
* Temperatuur: Hogere temperaturen verhogen doorgaans de corrosiesnelheid.
* pH: De pH van de omgeving kan de snelheid en het type corrosie beïnvloeden.
* Bescherming:
* Coatings: Net als ferrometalen kunnen coatings beschermen tegen omgevingsfactoren.
* Legering: Het toevoegen van elementen kan de corrosieweerstand van non-ferrometalen verbeteren.
* Anodische bescherming: Het toepassen van een gecontroleerde elektrische stroom op het metalen oppervlak om corrosie te onderdrukken.
Belangrijkste verschillen:
* Corrosieproduct: Roest in ferrometalen is poreus en maakt verdere corrosie mogelijk, terwijl oxidelagen op sommige non-ferrometalen als beschermende barrière kunnen fungeren.
* Mechanisme: Ferrometalen corroderen voornamelijk door elektrochemische processen, terwijl non-ferrometalen verschillende corrosiemechanismen kunnen hebben, afhankelijk van het metaal en de omgeving.
* Beschermingsmethoden: Sommige beschermingsmethoden, zoals galvanisatie, zijn specifiek voor ferrometalen, terwijl andere, zoals anodische bescherming, worden gebruikt voor non-ferrometalen.
Samengevat: Hoewel zowel ferro- als non-ferrometalen kunnen corroderen, verschillen hun corrosiemechanismen, producten en beschermingsmethoden aanzienlijk vanwege de unieke chemische eigenschappen van elk metaal. Het begrijpen van deze verschillen is cruciaal voor het kiezen van geschikte materialen en beschermingsmethoden voor verschillende toepassingen.
 Kobaltreactiviteit:eigenschappen, factoren en toepassingen
Kobaltreactiviteit:eigenschappen, factoren en toepassingen  Welke variabelen beïnvloeden de pH-waarden?
Welke variabelen beïnvloeden de pH-waarden?  De rol van de bovenbouw bij spanningsverlies in de eerste cyclus in lithium-ionbatterijen
De rol van de bovenbouw bij spanningsverlies in de eerste cyclus in lithium-ionbatterijen Techniek verdubbelt conversie van CO2 naar plastic component
Techniek verdubbelt conversie van CO2 naar plastic component Video:Wat zou Trump kunnen betekenen voor de chemie?
Video:Wat zou Trump kunnen betekenen voor de chemie?
 De natuurlijke comeback van tropische regenwouden in de savanneregio
De natuurlijke comeback van tropische regenwouden in de savanneregio Waarom proberen mensen middelen te behouden?
Waarom proberen mensen middelen te behouden?  Hoe vuur van vandaag het water van morgen zal beïnvloeden
Hoe vuur van vandaag het water van morgen zal beïnvloeden Rechtbank zegt dat het bevel om olieboringen in Everglades toe te staan ten onrechte is uitgevaardigd
Rechtbank zegt dat het bevel om olieboringen in Everglades toe te staan ten onrechte is uitgevaardigd Ozongat is zowel een succesverhaal voor het milieu als een wereldwijde bedreiging
Ozongat is zowel een succesverhaal voor het milieu als een wereldwijde bedreiging
Hoofdlijnen
- Een manier waarop eencellige organismen zichzelf beschermen tegen uitsterven is via een?
- Wie ontdekte het eten van vleesbacteriën?
- Onderzoekers laten zien hoe opportunistische bacteriën concurrenten verslaan
- Oorsprong van de term 'Eiwit':een korte geschiedenis
- Maak een lijst van prokaryotische cellen eukaryotisch en virussen in volgorde van toenemende complexiteit?
- Wat is het proces waarbij DNA wordt gedupliceerd?
- Wat is de opzettelijke verandering of overdracht van genetisch materiaal dat wordt genoemd?
- Een wetenschappelijke theorie kan het beste worden gedefinieerd als?
- Wat voor soort organismen zijn bacterieschimmels?
- Omkeerbare plakkerigheid in tandcement is iets om over te lachen
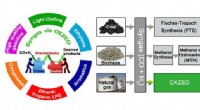
- Op oxide-zeoliet gebaseerd composietkatalysatorconcept maakt syngaschemie mogelijk die verder gaat dan Fischer-Tropsch-synthese
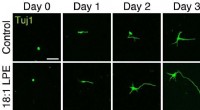
- Oleoyl-LPE oefent neurietstimulatie en neuroprotectie uit
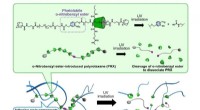
- Nieuwe AI-techniek kan leiden tot innovaties in biomaterialen

- Een nieuwe manier om verspild methaan te benutten
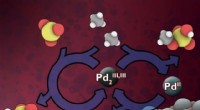
 Bij het meten van de dichtheid van een stof, waarom zou het belangrijk zijn om de substantie van de temperatuur vast te leggen?
Bij het meten van de dichtheid van een stof, waarom zou het belangrijk zijn om de substantie van de temperatuur vast te leggen?  Wat maken zilverstikstof en zuurstof?
Wat maken zilverstikstof en zuurstof?  Kerstconsumptie:wat zouden de grote economische filosofen denken?
Kerstconsumptie:wat zouden de grote economische filosofen denken?  Wat is schone kolentechnologie?
Wat is schone kolentechnologie?  Wat zijn de twee meest voorkomende temperatuurschalen?
Wat zijn de twee meest voorkomende temperatuurschalen?  Latijn kan studenten helpen hun moedertaal te overbruggen met Engels
Latijn kan studenten helpen hun moedertaal te overbruggen met Engels NASA's Spitzer Space Telescope beëindigt missie van astronomische ontdekking
NASA's Spitzer Space Telescope beëindigt missie van astronomische ontdekking Wat zijn enkele goede grappen over plaattektoniek?
Wat zijn enkele goede grappen over plaattektoniek?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

