
Wetenschap
Bereken de pH van een 2M kaliumhydroxideoplossing:een stapsgewijze handleiding
De concepten begrijpen
* KOH is een sterke basis: Dit betekent dat het volledig dissocieert in water, waardoor hydroxide-ionen (OH-) in oplossing komen.
* pH en pOH: pH meet de zuurgraad van een oplossing, terwijl pOH de basiciteit ervan meet. Ze zijn met elkaar verbonden door de vergelijking:pH + pOH =14
Berekeningen
1. Zoek de pOH:
* Omdat KOH een sterke base is, is de concentratie OH-ionen gelijk aan de concentratie KOH.
* Daarom [OH-] =2 M
* pOH =-log[OH-] =-log(2) ≈ -0,301
2. Bereken de pH:
* pH + pOH =14
* pH =14 - pOH =14 - (-0,301) ≈ 14,301
Resultaat
De pH van een 2M kaliumhydroxideoplossing is ongeveer 14,301 . Dit duidt op een zeer sterk basische oplossing.
Belangrijke opmerking:
* De pH-schaal is logaritmisch, wat betekent dat elke verandering in een geheel getal een tienvoudige verandering in zuurgraad of basiciteit vertegenwoordigt.
* Ga altijd voorzichtig om met sterke basen, aangezien deze ernstige brandwonden kunnen veroorzaken.
 Wat is de uitgebalanceerde vergelijking voor de reactie van salpeterzuur en natriumhydroxide?
Wat is de uitgebalanceerde vergelijking voor de reactie van salpeterzuur en natriumhydroxide?  Hoe zijn moleculen in een bepaalde vaste stof verschillend van de vorm van substantie -vloeistof?
Hoe zijn moleculen in een bepaalde vaste stof verschillend van de vorm van substantie -vloeistof?  Borium:het metalloïde met de kleinste atoomstraal
Borium:het metalloïde met de kleinste atoomstraal  Hoeveel mol ijzer zijn aanwezig in 3.15E24 Atoms Iron?
Hoeveel mol ijzer zijn aanwezig in 3.15E24 Atoms Iron?  Hoe zonlicht elektronen activeert om stikstof te breken en ammoniak te vormen
Hoe zonlicht elektronen activeert om stikstof te breken en ammoniak te vormen
 De uitstoot van lachgas kan erger worden naarmate het klimaat warmer wordt
De uitstoot van lachgas kan erger worden naarmate het klimaat warmer wordt Lasertechnologie meet biomassa in 's werelds grootste bomen
Lasertechnologie meet biomassa in 's werelds grootste bomen Waarom komt het douchegordijn op mij af?
Waarom komt het douchegordijn op mij af?  Welke soorten aperd op aarde frist?
Welke soorten aperd op aarde frist?  Onderzoek laat zien hoe de mensheid zich zou kunnen verenigen om mondiale uitdagingen aan te pakken
Onderzoek laat zien hoe de mensheid zich zou kunnen verenigen om mondiale uitdagingen aan te pakken
Hoofdlijnen
- Wat is het verschil tussen mitose van diercellen en plantenmitose?
- Wat is een set van drie uitspraken die de relatie tussen cellen en levende dingen samenvat?
- Wat maakt een held?
- Waar is de locatie van alle nucleïnezuren?
- Een geprioriteerde lijst van invasieve uitheemse soorten die het milieu van het VK bedreigen
- Welk hormoon produceert de T -cel?
- Bijenzoemen kunnen helpen bepalen hoe ze hun afnemende populatie kunnen redden
- Wat is een Dekadollar?
- Coyotes zijn hier om te verblijven in Noord-Amerikaanse steden. Hoe je ze van een afstand kunt waarderen
- Brug over gekoppelde wateren:wetenschappers 3D-printen volledig vloeibaar laboratorium op een chip
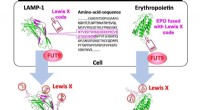
- Onderzoeksteam identificeert een moleculaire code die is ingebed in eiwit voor het reguleren van de glycosylering ervan
- Spinazie:chemie-experimenten tonen potentieel om brandstofcellen van stroom te voorzien

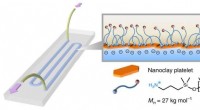
- Nieuwe supercondensors slaan elektrische lading op in textielmaterialen

- Hydrogel baant weg voor biomedische doorbraak

 Summit-supercomputer simuleert hoe mensen zullen remmen tijdens de landing op Mars
Summit-supercomputer simuleert hoe mensen zullen remmen tijdens de landing op Mars Hoeveel mensen geloven eigenlijk in astrologie?
Hoeveel mensen geloven eigenlijk in astrologie?  Dyson gaat elektrische auto bouwen in Singapore gericht op China
Dyson gaat elektrische auto bouwen in Singapore gericht op China Hoe komt ons Melkwegstelsel aan zijn spiraalvorm?
Hoe komt ons Melkwegstelsel aan zijn spiraalvorm? Horizontale beweging van lucht in relatie tot aardoppervlak?
Horizontale beweging van lucht in relatie tot aardoppervlak?  Wat gebeurt er als de aarde zijn baan verliest aan de maan?
Wat gebeurt er als de aarde zijn baan verliest aan de maan?  Nieuw materiaal kan kleine generatoren efficiënt van stroom voorzien
Nieuw materiaal kan kleine generatoren efficiënt van stroom voorzien Welk hemelse lichaam kan bij zonsopgang worden gezien als een heldere ster in de oostelijke hemel?
Welk hemelse lichaam kan bij zonsopgang worden gezien als een heldere ster in de oostelijke hemel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

