
Wetenschap
Chloor versus natriumreactiviteit:het verschil begrijpen
* Elektronegativiteit: Chloor heeft een hogere elektronegativiteit dan natrium. Dit betekent dat chloor een sterkere aantrekkingskracht heeft op elektronen.
* Elektronenconfiguratie: Chloor heeft 7 valentie-elektronen (elektronen in de buitenste schil). Er is nog één elektron nodig om een stabiele octetconfiguratie te bereiken. Natrium daarentegen heeft slechts 1 valentie-elektron. Het is gemakkelijker voor chloor om een elektron te verkrijgen dan voor natrium om er één te verliezen.
* Ionisatie-energie: Chloor heeft een hogere ionisatie-energie dan natrium. Dit betekent dat er meer energie nodig is om een elektron uit chloor te verwijderen dan voor natrium.
Reactiviteit in termen van het verkrijgen of verliezen van elektronen:
* Natrium: Natrium verliest gemakkelijk zijn ene valentie-elektron om een stabiele octetconfiguratie te bereiken, waarbij een positief ion (Na+) wordt gevormd. Dit maakt het een sterk reductiemiddel, wat betekent dat het gemakkelijk elektronen kan doneren.
* Chloor: Chloor krijgt gemakkelijk één elektron om een stabiele octetconfiguratie te bereiken, waarbij een negatief ion (Cl-) wordt gevormd. Dit maakt het een sterk oxidatiemiddel, wat betekent dat het gemakkelijk elektronen accepteert.
Samengevat: De hoge elektronegativiteit van chloor, de neiging om elektronen op te nemen en de hoge ionisatie-energie maken het veel reactiever dan natrium.
 Kaliumbromide is een stabiel molecuul Jodium een onstabiel Welke bewering verklaart het verschil in stabiliteit?
Kaliumbromide is een stabiel molecuul Jodium een onstabiel Welke bewering verklaart het verschil in stabiliteit?  Wat is ladingsscheiding over het bacteriële membraan?
Wat is ladingsscheiding over het bacteriële membraan?  Nieuw onderzoek laat zien hoe rechtbanken zich vaak verzetten tegen beschuldigingen van misbruik
Nieuw onderzoek laat zien hoe rechtbanken zich vaak verzetten tegen beschuldigingen van misbruik  Hoe Borax te converteren naar boorzuur
Hoe Borax te converteren naar boorzuur  Hoe zijn fotosynthese en koolstof gerelateerd?
Hoe zijn fotosynthese en koolstof gerelateerd?
 Onderzoekers:klimaatverandering zal de positie van de tropische regengordel van de aarde veranderen
Onderzoekers:klimaatverandering zal de positie van de tropische regengordel van de aarde veranderen Wetenschappers beschrijven de verspreiding van bodemmicro-organismen
Wetenschappers beschrijven de verspreiding van bodemmicro-organismen Een prijs zetten op koolstofvervuiling alleen zal waarschijnlijk niet helpen om de klimaatdoelen te bereiken
Een prijs zetten op koolstofvervuiling alleen zal waarschijnlijk niet helpen om de klimaatdoelen te bereiken Naarmate meer ontwikkelingslanden de export van plastic afval afwijzen, rijke landen zoeken thuis oplossingen
Naarmate meer ontwikkelingslanden de export van plastic afval afwijzen, rijke landen zoeken thuis oplossingen De oorzaken en gevolgen van Tornado's
De oorzaken en gevolgen van Tornado's
Hoofdlijnen
- Welke dierencel heeft geen kern?
- Wat is het eerste nucleïnezuursysteem dat moet worden gevormd?
- Zijn alle schimmels diploïde en bevatten ze chromosomen van beide ouders?
- Hoe kunnen verbindingen in verschillende soorten organismen worden gebruikt om mensen ten goede te komen?
- Wat zijn 5 voorbeelden van eukaryoten?
- Wanneer houdt de verspreiding van voedingsstoffen onder cellen een organisme op?
- Welk proces wordt gedacht dat het betrokken is bij het ontstaan van eukaryoten van prokaryoten?
- Wat komt de plant binnen via zijn wortels?
- Wat wordt voornamelijk gevormd uit dode cellen?
- Voedselverspilling omzetten in bioplastics

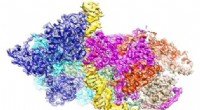
- Hi-res afbeelding van structuur van het oorsprongherkenningscomplex gebonden aan DNA onthuld
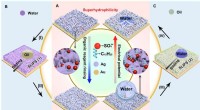
- Elektrolytisch gedeponeerde oppervlakken met omkeerbaar schakelende grensvlakeigenschappen
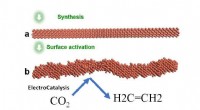
- Onderzoekers ontdekken effectieve manier om koolstofdioxide om te zetten in ethyleen
- Het minimaliseren van brandstofexplosies en branden door ongelukken en terroristische daden met polymeren

 Nieuwe op koolstof gebaseerde afstembare metasurface-absorber maakt de weg vrij voor geavanceerde terahertz-technologie
Nieuwe op koolstof gebaseerde afstembare metasurface-absorber maakt de weg vrij voor geavanceerde terahertz-technologie  Wat zijn de weefsels die combineren om een orgel te vormen?
Wat zijn de weefsels die combineren om een orgel te vormen?  Voorbij sociale netwerken:hoe culturele overtuigingen zich werkelijk verspreiden
Voorbij sociale netwerken:hoe culturele overtuigingen zich werkelijk verspreiden  Wat is het dichtste deel van een atoom?
Wat is het dichtste deel van een atoom?  Wat houdt een isolator de elektriciteit in?
Wat houdt een isolator de elektriciteit in?  Biotische factoren voor een jachtluipaard
Biotische factoren voor een jachtluipaard  Wat is een lage nok van rotsen zand en grond achtergelaten door Glacier?
Wat is een lage nok van rotsen zand en grond achtergelaten door Glacier?  Wat zijn de kenmerken die alle vloeistoffen delen?
Wat zijn de kenmerken die alle vloeistoffen delen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

