
Wetenschap
Zwavelzuur- en natriumhydroxide-neutralisatie:vergelijking en uitleg
H₂SO₄ (waterig) + 2NaOH (waterig) → Na₂SO₄ (waterig) + 2H₂O (l)
Hier is een overzicht:
* H₂SO₄ (aq): Zwavelzuur, in waterige (opgelost in water) toestand.
* NaOH (aq): Natriumhydroxide, ook in waterige toestand.
* Na₂SO₄ (aq): Natriumsulfaat, het zout dat als product wordt gevormd, in waterige toestand.
* 2H₂O (l): Water, het andere product van de reactie, in vloeibare toestand.
Uitleg:
* Neutralisatie: Deze reactie wordt beschouwd als een neutralisatiereactie omdat het sterke zuur (H₂SO₄) en de sterke base (NaOH) reageren en een neutraal zout (Na₂SO₄) en water vormen.
* Stoichiometrie: De vergelijking is in evenwicht, wat betekent dat het aantal atomen van elk element aan beide zijden gelijk is. Merk op dat we twee mol NaOH nodig hebben om te reageren met één mol H₂SO₄, omdat zwavelzuur een diprotisch zuur is, wat betekent dat het twee protonen (H⁺-ionen) kan doneren.
Deze reactie is zeer exotherm, wat betekent dat er warmte vrijkomt, en kan in verschillende toepassingen worden gebruikt, waaronder:
* Titratie: Bepalen van de concentratie van een zuur- of base-oplossing.
* Chemische synthese: Productie van natriumsulfaat, dat verschillende industriële toepassingen kent.
* Afvalwaterzuivering: Neutraliseren van zuur afvalwater.
 Fluorescerende moleculen onthuld door kwantumchemie en machine learning
Fluorescerende moleculen onthuld door kwantumchemie en machine learning Uit welke elementen bestaat Na Cl?
Uit welke elementen bestaat Na Cl?  Hoeveel moleculen zijn aanwezig in één gram waterstof?
Hoeveel moleculen zijn aanwezig in één gram waterstof?  Wat kun je vaststellen over een atoom op basis van zijn atoomstraal?
Wat kun je vaststellen over een atoom op basis van zijn atoomstraal?  Wat is een manier om valentie-elektronen in een ionische verbinding bij te houden?
Wat is een manier om valentie-elektronen in een ionische verbinding bij te houden?
 Klimaatrecords worden steeds weer verbroken. Dit is wat u moet weten
Klimaatrecords worden steeds weer verbroken. Dit is wat u moet weten  Nieuwe methode om microplastics onder onze voeten op te sporen
Nieuwe methode om microplastics onder onze voeten op te sporen Afvalwaterzuiveringssysteem wint elektriciteit terug, filtert water
Afvalwaterzuiveringssysteem wint elektriciteit terug, filtert water Belangrijke fasen van de menselijke evolutie vallen samen met flikkeringen in het klimaat van Oost-Afrika
Belangrijke fasen van de menselijke evolutie vallen samen met flikkeringen in het klimaat van Oost-Afrika Kunnen nieuwe technologieën Europa helpen de smaak voor insecten te proeven?
Kunnen nieuwe technologieën Europa helpen de smaak voor insecten te proeven?
Hoofdlijnen
- Wat is diploïde eukaryotisch?
- Waarom zijn bacteriën het meest zorgwekkend?
- Door zich te hechten aan het lichaam van een walvisjucca -motten kunnen worden voeden terwijl ze door voedingsrijk rijk water waar of onwaar beweegt?
- Nieuwe studie onthult hoe menselijk embryo de voorloper van bloedvormende stamcellen ontwikkelt
- Welke organismen hebben cellen die organellen bevatten?
- Hoeveel chromosomen heeft een somatische cel in de mens?
- Wat is Cell Furrow?
- Wat zijn drie uitspraken die alle levende dingen definiëren in termen van cellen?
- Wat zijn de 3 soorten reproductieve klonen?
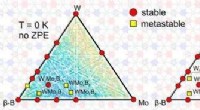
- Wetenschappers voorspellen nieuwe, moeilijk, en superharde ternaire verbindingen
- Op zoek naar verborgen toestanden van het COVID-19 spike-eiwit

- Primaire bronnen van chloorfluorkoolwaterstoffen (CFK's) en hun impact op de ozonlaag

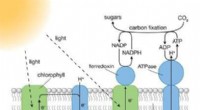
- Wetenschappers ontwerpen moleculair systeem voor kunstmatige fotosynthese
- Uitvinding van piepkleine organische films kan nieuwe elektronica mogelijk maken

 Australië maakt zich op voor het ergste nu het bosbrandseizoen vroeg begint
Australië maakt zich op voor het ergste nu het bosbrandseizoen vroeg begint Stroom uit de zee? Tribo-elektrische nanogenerator extraheert energie-oceaangolven
Stroom uit de zee? Tribo-elektrische nanogenerator extraheert energie-oceaangolven  RiverProAnalysis, een open-source set Matlab-scripts voor longitudinale profielanalyse van rivieren
RiverProAnalysis, een open-source set Matlab-scripts voor longitudinale profielanalyse van rivieren Wat is het woordvergelijking voor zink die met stoom reageert?
Wat is het woordvergelijking voor zink die met stoom reageert?  Wat heeft de bijnaam de krachtpatser van de cel en die betrokken is bij de energieproductie voor cellen?
Wat heeft de bijnaam de krachtpatser van de cel en die betrokken is bij de energieproductie voor cellen?  Waar vindt de lichtafhankelijke fase plaats in planten?
Waar vindt de lichtafhankelijke fase plaats in planten?  Wanneer elektromagnetische energie van lucht naar water reist, zijn de golven gebogen vanwege de dichtheidsverschillen tussen en wat wordt deze buiging genoemd?
Wanneer elektromagnetische energie van lucht naar water reist, zijn de golven gebogen vanwege de dichtheidsverschillen tussen en wat wordt deze buiging genoemd?  Chaotisch klimaat, chaotische steden voeden de tol van overstromingen in Brazilië
Chaotisch klimaat, chaotische steden voeden de tol van overstromingen in Brazilië
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

