
Wetenschap
Natrium- en chloorbinding:ionisch versus covalent
* Natrium (Na) is een metaal en heeft een lage ionisatie-energie, wat betekent dat het gemakkelijk zijn buitenste elektron verliest en een positief geladen ion (Na+) wordt.
* Chloor (Cl) is een niet-metaal en heeft een hoge elektronenaffiniteit, wat betekent dat het gemakkelijk een elektron verkrijgt om een negatief geladen ion (Cl-) te worden.
Wanneer natrium en chloor reageren, doneert natrium zijn elektron aan chloor. Deze overdracht van elektronen creëert een elektrostatische aantrekkingskracht tussen de tegengesteld geladen ionen, wat resulteert in de vorming van een ionische binding. De resulterende verbinding, natriumchloride (NaCl), is een kristalrooster dat bij elkaar wordt gehouden door deze ionische bindingen.
Belangrijkste verschillen tussen covalente en ionische bindingen:
* Covalente obligaties: Betrek het delen van elektronen tussen atomen.
* Ionische bindingen: Betreft de overdracht van elektronen tussen atomen, resulterend in de vorming van ionen die bij elkaar worden gehouden door elektrostatische aantrekking.
 Welke redenen verklaren het beste waarom de aarde zoveel biomen heeft?
Welke redenen verklaren het beste waarom de aarde zoveel biomen heeft?  10 veerkrachtige toendraplanten die gedijen in extreme kou
10 veerkrachtige toendraplanten die gedijen in extreme kou  Onderzoek zal landbeheerders helpen bij het nemen van een risicoanalyse-aanpak voor de nieuwe natuurbrandrealiteit
Onderzoek zal landbeheerders helpen bij het nemen van een risicoanalyse-aanpak voor de nieuwe natuurbrandrealiteit Algoritme om motregen-turbulentie-interacties vast te leggen, zou de voorspellingen van toekomstige klimaatomstandigheden kunnen verbeteren
Algoritme om motregen-turbulentie-interacties vast te leggen, zou de voorspellingen van toekomstige klimaatomstandigheden kunnen verbeteren De echte mislukking van de klimaatconferenties in Madrid was het niet krijgen van een brede deal over de wereldwijde koolstofmarkten
De echte mislukking van de klimaatconferenties in Madrid was het niet krijgen van een brede deal over de wereldwijde koolstofmarkten
Hoofdlijnen
- Wat veroorzaakt de grote verscheidenheid aan mogelijke gencombinaties van nakomelingen van twee ouders?
- Wat is eiwit en hoe het heeft gemaakt?
- Wat betekent variabele in een wetenschappelijke methode?
- De beste definitie van een waarblijvende plant is er een die?
- Wanneer u uitlegt wat heeft waargenomen, leidt u af aan het classificeren?
- Welke manier zijn alle levende organismen op aarde vergelijkbaar?
- De gecontroleerde timing van genexpressie is cruciaal voor een organisme omdat het ervoor zorgt welke het volgende?
- Genezing van verbrande poten met vissenhuid
- Nieuwe studie onderzoekt hoe overtuigingen en politieke voorkeuren het begrip van het publiek over raciale ongelijkheid vormen
- Onderzoekers onderzoeken materiaaleigenschappen voor langduriger, efficiëntere zonnecellen

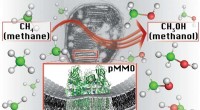
- Methaanverbruikende bacteriën kunnen de brandstof van de toekomst zijn
- Een nieuwe manier om zachte robots te maken:DNA-triggers die ervoor zorgen dat hydrogels van vorm veranderen

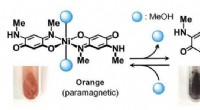
- Nieuw type sensormateriaal ontwikkeld
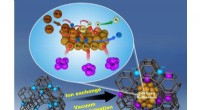
- Ammoniakafbraak voor waterstofeconomie, verbetering van de efficiëntie van waterstofextractie
 Welke wetenschappers drukken uit wat er tijdens de fotosynthese gebeurt met behulp van deze chemische vergelijking?
Welke wetenschappers drukken uit wat er tijdens de fotosynthese gebeurt met behulp van deze chemische vergelijking?  Typen spinnen in Michigans Upper Peninsula
Typen spinnen in Michigans Upper Peninsula Facebooks controversiële Portal-videochatapparaat krijgt browser, games:het maakt misschien niet uit
Facebooks controversiële Portal-videochatapparaat krijgt browser, games:het maakt misschien niet uit Is een gewoon een groot grasveld?
Is een gewoon een groot grasveld?  Welke golf draagt de meeste energie?
Welke golf draagt de meeste energie?  Het buigen van een organische halfgeleider kan de elektrische stroom stimuleren
Het buigen van een organische halfgeleider kan de elektrische stroom stimuleren Duitsland klampt zich vast aan diesel, zelfs toen de eerste rijverboden toesloegen
Duitsland klampt zich vast aan diesel, zelfs toen de eerste rijverboden toesloegen Hoe heet is planeet Mars?
Hoe heet is planeet Mars?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

