
Wetenschap
Stoichiometrieberekening:volume BaCl2 nodig voor volledige reactie met Na2SO4
1. Bepaal het aantal mol Na₂SO₄:
* Mol =Molariteit x Volume (in liters)
* Mol Na₂SO₄ =0,453 M x (42,0 ml / 1000 ml/l) =0,01903 mol
2. Gebruik de stoichiometrie van de reactie:
* Uit de gebalanceerde netto ionische vergelijking zien we dat 1 mol Ba²⁺ reageert met 1 mol SO₄²⁻ om 1 mol BaSO₄ te vormen.
* Daarom hebben we 0,01903 mol BaCl₂ nodig om volledig met Na₂SO₄ te reageren.
3. Bereken het volume van de BaCl₂-oplossing:
* Volume =Mol / Molariteit
* Volume BaCl₂ =0,01903 mol / 0,131 M =0,145 L
* Omrekenen naar milliliter:0,145 l x 1000 ml/l =145 ml
Je hebt dus 145 ml 0,131 M BaCl₂ nodig om volledig te reageren met 42,0 ml 0,453 M Na₂SO₄.
 Waarom voedingskeuzes een impact hebben op de wereldwijde fauna en menselijke populaties
Waarom voedingskeuzes een impact hebben op de wereldwijde fauna en menselijke populaties NASA ziet Systeem 91P samenkomen ten oosten van Queensland
NASA ziet Systeem 91P samenkomen ten oosten van Queensland 38 doden door toenemende overstromingen in Mozambique na tweede cycloon
38 doden door toenemende overstromingen in Mozambique na tweede cycloon Beschrijf de vijf niveaus van ecologische studie?
Beschrijf de vijf niveaus van ecologische studie?  De verschillen tussen een land en een continent
De verschillen tussen een land en een continent
Hoofdlijnen
- Waar is het fenotype van een dier dat van is gemaakt?
- Relatie tussen één gen en polypeptide?
- Wat is de Thermosophere -laag?
- Welke van de volgende is een methode reproductie die over het algemeen zeer snel optreedt?
- Hoe ziet een moleculaire frequentiediscriminator eruit?
- Een geslacht van Europese papierwespen voor het eerst herzien met behulp van integratieve taxonomie
- Celdood:hoe een eiwit immuuncellen tot zelfmoord drijft
- Wat zijn de 3 wetenschappelijke variabelen?
- Wat bevatten organismen?
- Wat zit er in deze plant? Het beste geautomatiseerde systeem voor het vinden van potentiële medicijnen

- Op tandwielen gebaseerde mechanische metamaterialen maken het mogelijk om configureerbare bladen te maken
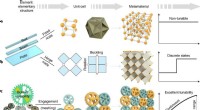
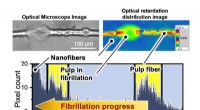
- Het bepalen van de verslanking van houtpulp
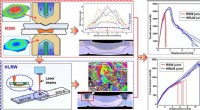
- Onderzoekers verbeteren de mechanische eigenschappen van aluminium/stalen verbindingen
- Forensische wetenschappers herstellen menselijk DNA van muggen

 Wat zijn de namen van in het lichaam?
Wat zijn de namen van in het lichaam?  Hoe de popcultuur de juridische opvattingen over vloeken kan (en moet) veranderen
Hoe de popcultuur de juridische opvattingen over vloeken kan (en moet) veranderen  Hoe beïnvloedt de hydrosfeer igneusgesteenten?
Hoe beïnvloedt de hydrosfeer igneusgesteenten?  Het cytoskelet begrijpen:een geschiedenis van ontdekkingen
Het cytoskelet begrijpen:een geschiedenis van ontdekkingen  Waarom komt de zon op in het oosten en gaat het westen onder?
Waarom komt de zon op in het oosten en gaat het westen onder?  Hoe proportioneel te berekenen voor normale verdeling
Hoe proportioneel te berekenen voor normale verdeling Nieuwe methode gevonden om kleine kunstmatige zwemmers te verplaatsen
Nieuwe methode gevonden om kleine kunstmatige zwemmers te verplaatsen Spaceship 1 en Spaceship 2 hebben gelijke massa's van 300 kg hebben een snelheid 0 ms 6 als ze tegen elkaar botsen, wat is het gecombineerde momentum?
Spaceship 1 en Spaceship 2 hebben gelijke massa's van 300 kg hebben een snelheid 0 ms 6 als ze tegen elkaar botsen, wat is het gecombineerde momentum?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

