
Wetenschap
Permanganaatoxidatie van chloride:een gedetailleerde redoxreactie
Hier is de gebalanceerde redoxreactie:
2MnO₄⁻(aq) + 10Cl⁻(aq) + 16H⁺(aq) → 2Mn²⁺(aq) + 5Cl₂(g) + 8H₂O(l)
Uitleg:
* Oxidatie: Chloride-ionen (Cl⁻) worden geoxideerd tot chloorgas (Cl₂). Elk chloride-ion verliest één elektron om chloorgas te vormen.
* Reductie: Permanganaationen (MnO₄⁻) worden gereduceerd tot mangaan(II)-ionen (Mn²⁺). Elk permanganaat-ion krijgt vijf elektronen en de oxidatietoestand verandert van +7 naar +2.
* Zuur medium: De reactie vereist een zuur medium (H⁺) om de noodzakelijke protonen te leveren voor de reductie van permanganaationen en de vorming van water.
Voorwaarden:
* Zure oplossing: De reactie verloopt gemakkelijk in zure oplossingen, zoals verdund zwavelzuur.
* Concentratie: De concentratie van de reactanten speelt een rol in de reactiesnelheid. Hogere concentraties leiden doorgaans tot snellere reacties.
* Temperatuur: De reactiesnelheid neemt toe met de temperatuur.
Opmerkingen:
* De oplossing verandert van paars (MnO₄⁻) naar kleurloos (Mn²⁺) naarmate de permanganaationen worden gereduceerd.
*De karakteristieke scherpe geur van chloorgas (Cl₂) wordt waargenomen.
Opmerking: Deze reactie is een klassiek voorbeeld van een redoxreactie waarbij een sterk oxidatiemiddel (permanganaat) een zwakker oxidatiemiddel (chloride) oxideert.
 Water is een voorbeeld van welke verbinding?
Water is een voorbeeld van welke verbinding?  Is chloorgas een homogeen mengsel?
Is chloorgas een homogeen mengsel?  Welke elementen zijn stabiele neon koolstofboor of fluor?
Welke elementen zijn stabiele neon koolstofboor of fluor?  Wat is de naam van hij wetenschapper die ontdekte dat atomen positieve aanklacht hebben?
Wat is de naam van hij wetenschapper die ontdekte dat atomen positieve aanklacht hebben?  Een bijgewerkt begrip van hoe chemicaliën met toegevoegde waarde kunnen worden gesynthetiseerd
Een bijgewerkt begrip van hoe chemicaliën met toegevoegde waarde kunnen worden gesynthetiseerd
Hoofdlijnen
- Hebben bactriumcellen ATP nodig voor flagella -beweging?
- Hoe is eiwitsynthese gerelateerd aan genexpressie?
- Organismen die ernstige omgeving kunnen overleven?
- Wat doet het cyptoplasma?
- Geen microben? probleem voor rupsen
- Wat is de celstructuur die een plantencel stijver maakt dan een dierlijke cel?
- Gebaseerd op de samenstelling van het floëemweefsel, waarvoor wordt het hoogstwaarschijnlijk door de plant gebruikt?
- Wetenschappers krijgen een beter beeld van hoe ooglenseiwitten worden gesorteerd
- Wat is de functie van sporen?
- Chemische reacties doorbreken energiebarrières met behulp van flyby-trajecten
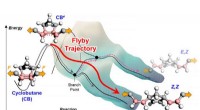
- Inzichten op atoomniveau verkregen voor een belangrijk lipidenbindend eiwit dat betrokken is bij kanker
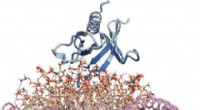
- Hoe u de bicarbonaatconcentratie kunt berekenen op basis van de partiële CO₂-druk

- Nieuwe techniek belooft verbeterde detectie van uitgezaaide prostaatkanker
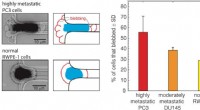
- Nieuw ontdekt quasikristal werd gecreëerd door de eerste nucleaire explosie op Trinity Site

 Welke kracht moet worden gebruikt om 224 joulen werk te doen op een object over een afstand van 32 meter?
Welke kracht moet worden gebruikt om 224 joulen werk te doen op een object over een afstand van 32 meter?  Hoe zal een object bewegen dat met de minste hoeveelheid kracht wordt getrokken?
Hoe zal een object bewegen dat met de minste hoeveelheid kracht wordt getrokken?  Twitter trekt politieke advertenties terug, maar valkuilen wachten
Twitter trekt politieke advertenties terug, maar valkuilen wachten Als een vliegtuig 200 m per s in tegenwind van 50m vliegt, wat is de resulterende snelheid?
Als een vliegtuig 200 m per s in tegenwind van 50m vliegt, wat is de resulterende snelheid?  Uranium ter vervanging van plastic? Een doorbraak in de chemie kan de weg vrijmaken voor nieuwe materialen
Uranium ter vervanging van plastic? Een doorbraak in de chemie kan de weg vrijmaken voor nieuwe materialen  Smog dwingt inwoners van Peking om te innoveren voor de wereld
Smog dwingt inwoners van Peking om te innoveren voor de wereld Waarom worden planten buiten beter?
Waarom worden planten buiten beter?  Als ET belt, kunnen we er dan zeker van zijn dat we niet worden vervalst?
Als ET belt, kunnen we er dan zeker van zijn dat we niet worden vervalst?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

