
Wetenschap
Covalente obligaties:het delen van elektronen en moleculaire stabiliteit begrijpen
* Atomen zoeken stabiliteit: Atomen zijn het meest stabiel als hun buitenste elektronenschil (valentieschil) vol is. Dit betekent meestal dat er 8 elektronen zijn (octetregel).
* Elektronen delen: Atomen met onvolledige buitenste schillen kunnen stabiliteit bereiken door elektronen te delen met andere atomen.
* Vorming van covalente bindingen: Dit gedeelde elektronenpaar vormt een covalente binding en houdt de twee atomen bij elkaar.
* Stabiliteit en molecuulvorming: De gedeelde elektronen worden aangetrokken door beide kernen, waardoor een sterke elektrostatische kracht ontstaat die de atomen in een vaste opstelling houdt en een molecuul vormt.
Voorbeeld:
* Een waterstofatoom (H) heeft één elektron in de buitenste schil en heeft er nog één nodig om stabiel te zijn.
* Twee waterstofatomen kunnen hun afzonderlijke elektronen delen, waardoor een covalente binding ontstaat en een waterstofmolecuul (H₂) ontstaat.
Belangrijkste punten:
* Covalente bindingen zijn over het algemeen sterker dan ionische bindingen.
* Covalente bindingen kunnen enkelvoudig, dubbel of drievoudig zijn, afhankelijk van het aantal gedeelde elektronen.
* Covalente binding is verantwoordelijk voor de vorming van een breed scala aan moleculen, van eenvoudige moleculen zoals water (H₂O) tot complexe biologische moleculen zoals DNA.
 Hoe efficiënt smelt zout ijs?
Hoe efficiënt smelt zout ijs?  Wat is verdunde oplossing en concentratie?
Wat is verdunde oplossing en concentratie?  Verbinding gevonden in bomen heeft de potentie om resistente bacteriën te doden
Verbinding gevonden in bomen heeft de potentie om resistente bacteriën te doden Wat zijn de subatomaire deeltjes die de basisstructuur vormen van atomen die worden genoemd?
Wat zijn de subatomaire deeltjes die de basisstructuur vormen van atomen die worden genoemd?  Nieuwe methode voor hydroborering van alkynen:Radicalen induceren ongebruikelijke selectiviteit
Nieuwe methode voor hydroborering van alkynen:Radicalen induceren ongebruikelijke selectiviteit
 Magnitude 5.3 aardbeving slaat toe voor de kust van Zuid-Californië
Magnitude 5.3 aardbeving slaat toe voor de kust van Zuid-Californië Wat is remanentie?
Wat is remanentie?  Waarom is licht geen vorm van materie?
Waarom is licht geen vorm van materie?  Hoe worden planten aangepast aan zandduinomgeving?
Hoe worden planten aangepast aan zandduinomgeving?  DDT-verontreinigende stoffen die in diepzeevissen voor de kust van LA worden aangetroffen, roepen vragen op over de voortdurende bedreiging van de pesticiden voor wilde dieren
DDT-verontreinigende stoffen die in diepzeevissen voor de kust van LA worden aangetroffen, roepen vragen op over de voortdurende bedreiging van de pesticiden voor wilde dieren
Hoofdlijnen
- Welk koolhydraatmonomeer is de meest voorkomende in levende organismen?
- Cilia in eencellige organismen:functies en belang
- Eerste foto's van BRCA2-eiwit laten zien hoe het werkt om DNA te repareren
- Kleine moleculen behouden stamcellen:Onderzoekers laten zien wat constante plantengroei mogelijk maakt
- Wat is een bacterieorganisme dat dode organisme eet?
- Wat zijn de twee reacties van aerobe cellulaire ademhaling?
- Hoe gebruiken zeester mitose?
- Wetenschappers volgen aseksuele kleine wormen - waarvan de afstamming 18 miljoen jaar teruggaat
- Uit welke xyleemcellen bestaat het grootste deel van hout?
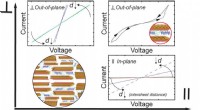
- Zelfmontage, biomimetische composieten hebben ongebruikelijke elektrische eigenschappen
- Berekening van het massapercentage waterstof in water:11,19% uitgelegd

- Bladgoud kan helpen bij het diagnosticeren van virale infecties in instellingen met weinig middelen

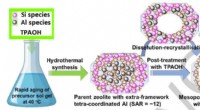
- Onderzoekers ontwikkelen holle ZSM-5 zeolietkatalysator met een lage verhouding tussen silicium en aluminium
- Chirurgische instrumenten maken van medisch afval
 Terwijl de energie in golven door het water beweegt?
Terwijl de energie in golven door het water beweegt?  Welke twee dingen beïnvloeden of bepalen de hoeveelheid zwaartekracht in een object?
Welke twee dingen beïnvloeden of bepalen de hoeveelheid zwaartekracht in een object?  Klauwen of niet klauwen? Het kattenvoorstel uit New York leidt tot een speels debat
Klauwen of niet klauwen? Het kattenvoorstel uit New York leidt tot een speels debat  Waarom wordt Orion gezien in de zomerhemel?
Waarom wordt Orion gezien in de zomerhemel?  Hoeveel atomen in ijzersulfaat?
Hoeveel atomen in ijzersulfaat?  Isotopische analyses koppelen de levens van laat-neolithische individuen aan de begraafplaats in Spanje
Isotopische analyses koppelen de levens van laat-neolithische individuen aan de begraafplaats in Spanje Chemische thermometers brengen temperatuur op nanometerschaal
Chemische thermometers brengen temperatuur op nanometerschaal Welke reactie produceert water als bijproduct?
Welke reactie produceert water als bijproduct?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

