
Wetenschap
Edelgassen:waarom ze geen verbindingen vormen en opmerkelijke voorbeelden
* Helium (hij)
* Neon (Ne)
* Argon (Ar)
* Krypton (Kr)
* Xenon (Xe)
* Radon (Rn)
Waarom vormen edelgassen geen verbindingen?
Edelgassen hebben een volledige buitenste schil van elektronen, waardoor ze zeer stabiel en niet-reactief zijn. Ze hebben niet de neiging om elektronen te winnen, te verliezen of te delen om chemische bindingen te vormen. Daarom worden ze ‘inerte gassen’ genoemd.
Uitzonderingen:
Hoewel edelgassen over het algemeen niet reactief zijn, zijn er enkele uitzonderingen:
* Xenon en krypton kan onder specifieke omstandigheden verbindingen vormen met zeer elektronegatieve elementen zoals fluor en zuurstof.
* Radon is radioactief en heeft een korte halfwaardetijd, dus de reactiviteit ervan is niet goed bestudeerd.
Hoewel de term 'inerte gassen' niet helemaal juist is, worden edelgassen daarom nog steeds beschouwd als de elementen die normaal gesproken geen verbindingen vormen.
 Bladgoud kan helpen bij het diagnosticeren van virale infecties in instellingen met weinig middelen
Bladgoud kan helpen bij het diagnosticeren van virale infecties in instellingen met weinig middelen Hoe heet de vloeistof in een thermometer?
Hoe heet de vloeistof in een thermometer?  Hoe beïnvloedt een verhoogde pH het zuurstofniveau?
Hoe beïnvloedt een verhoogde pH het zuurstofniveau?  Wat is de juiste formule voor verbinding gevormd uit MG en S?
Wat is de juiste formule voor verbinding gevormd uit MG en S?  Geleidt elektriciteit in metaal van vaste toestand of niet -metaal?
Geleidt elektriciteit in metaal van vaste toestand of niet -metaal?
 Satelliet ziet rook van meerdere branden in New Mexico
Satelliet ziet rook van meerdere branden in New Mexico Houtskoolresten kunnen CO2-uitstoot versnellen na bosbranden
Houtskoolresten kunnen CO2-uitstoot versnellen na bosbranden Zuid-Afrika Kaapstad versoepelt waterrantsoenering
Zuid-Afrika Kaapstad versoepelt waterrantsoenering Speciale uitgave om klimaatwetenschap voor servicepartnerschap tussen China en het VK onder de aandacht te brengen
Speciale uitgave om klimaatwetenschap voor servicepartnerschap tussen China en het VK onder de aandacht te brengen Wat voor soort gevaarlijke planten leven in Fiji?
Wat voor soort gevaarlijke planten leven in Fiji?
Hoofdlijnen
- Welke van de volgende is het meest waarschijnlijk het gevolg van een organisme met lipiden in zijn lichaam?
- Wat is de functie van stam in planten?
- Wat is de rol van integrines?
- Wat wordt aangetroffen, zowel planten- als dierlijke cellen zoals gelei?
- Wat zijn de functies van fysiologische dode ruimte?
- Wat is hematapoiese?
- Wat zou er gebeuren als de celcyclus normaal zou verlopen, behalve dat cytokinese niet plaatsvond?
- Wie zei dat dat protoplasma de fysieke basis van het leven is?
- Wat zijn enkele namen voor wetenschapsboeken?
- Nieuwe vormgeheugenlegering ontdekt door middel van kunstmatige intelligentie
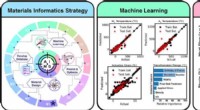
- Vooruitgang in de richting van het aansluiten van een antibioticapomp

- Een composietmateriaal van organogelator-cellulose voor praktisch en milieuvriendelijk herstel van olievlekken op zee
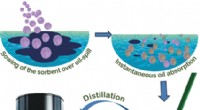
- Polymeer gloeit omkeerbaar wit wanneer uitgerekt

- Chemische golven gids voor katalysatoren van de toekomst
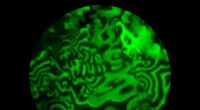
 Hoe voelen insecten de hitte?
Hoe voelen insecten de hitte?  Hoe verzorgers kunnen helpen bij het ontwikkelen van de opkomende taalvaardigheden van kinderen
Hoe verzorgers kunnen helpen bij het ontwikkelen van de opkomende taalvaardigheden van kinderen Welke van twee verschillende soorten gebeurt proberen dezelfde niche te bezetten?
Welke van twee verschillende soorten gebeurt proberen dezelfde niche te bezetten?  Wanneer zwavel brandt, vormt het een alkalisch gas?
Wanneer zwavel brandt, vormt het een alkalisch gas?  Is Table Mountain een vulkanische berg?
Is Table Mountain een vulkanische berg?  Boortrifluoride (BF₃):formule, eigenschappen en uitleg
Boortrifluoride (BF₃):formule, eigenschappen en uitleg  Klimaatchaos vermijden betekent ongekende verandering:VN-rapport
Klimaatchaos vermijden betekent ongekende verandering:VN-rapport Wat is de betekenis van synoniemen een voorbeeld geven?
Wat is de betekenis van synoniemen een voorbeeld geven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

