
Wetenschap
Zuren:definitie, eigenschappen en hoe ze waterstofionen vrijgeven
Hier is een overzicht:
* Zuren zijn chemische verbindingen die protonen (H+) aan andere stoffen doneren.
* Waterstofionen (H+) zijn positief geladen ionen die worden gevormd wanneer een waterstofatoom zijn elektron verliest.
* Waterige oplossing verwijst naar een oplossing waarbij water het oplosmiddel is.
Wanneer een zuur in water oplost, doneert het H+-ionen aan de watermoleculen. Dit resulteert in een toename van de concentratie H+-ionen in de oplossing, waardoor de oplossing zuur wordt.
Voorbeelden van zuren:
* Zoutzuur (HCl): Gevonden in maagzuur, gebruikt in industriële processen.
* Zwavelzuur (H2SO4): Gebruikt in batterijen, meststoffen en veel industriële processen.
* Salpeterzuur (HNO3): Gebruikt bij de productie van kunstmest, explosieven en kunststoffen.
* Azijnzuur (CH3COOH): Gevonden in azijn.
De sterkte van een zuur wordt bepaald door hoe gemakkelijk het H+-ionen afgeeft. Sterke zuren geven H+-ionen volledig af, terwijl zwakke zuren slechts een klein deel van hun H+-ionen vrijgeven.
 Kun je me een exanple geven van slogan over chemie?
Kun je me een exanple geven van slogan over chemie?  Onderzoekers vorderen inspanningen om glyfosaatpesticide in haver nauwkeurig te meten
Onderzoekers vorderen inspanningen om glyfosaatpesticide in haver nauwkeurig te meten Wat zijn twee manieren om de isotoop van bromide te schrijven die 10 meer neutronen heeft dan het atoomnummer?
Wat zijn twee manieren om de isotoop van bromide te schrijven die 10 meer neutronen heeft dan het atoomnummer?  Is KF een zuur of een basis?
Is KF een zuur of een basis?  Hoe kunnen wetenschappers de innerlijke structuur van een atoom bestuderen?
Hoe kunnen wetenschappers de innerlijke structuur van een atoom bestuderen?
 Nieuwe analyse laat zien dat de mondiale zoetwatercyclus veel verder is verschoven dan de pre-industriële omstandigheden
Nieuwe analyse laat zien dat de mondiale zoetwatercyclus veel verder is verschoven dan de pre-industriële omstandigheden  NASA-NOAA-satellieten kijken 's nachts naar tropische storm Kiko
NASA-NOAA-satellieten kijken 's nachts naar tropische storm Kiko Hoe is Plastic Trash van invloed op de Ocean Food Chain?
Hoe is Plastic Trash van invloed op de Ocean Food Chain?  Dodental bevriezen Europa stijgt tot 65
Dodental bevriezen Europa stijgt tot 65 Waarom bloeit plankton? Het antwoord zou een heroverweging van het voedselweb van de oceaan kunnen afdwingen
Waarom bloeit plankton? Het antwoord zou een heroverweging van het voedselweb van de oceaan kunnen afdwingen
Hoofdlijnen
- Kan een kunstneus voedselbederf detecteren?
- Welke cellen stoppen met delen wanneer ze volwassen worden?
- Welk type celorganel is in structuur vergelijkbaar met een radiator?
- Gedachtenexperiment:wat is ons transhumane pad voorbij de aarde?
- Welke vervuiling wordt het genoemd wanneer bij een onderzoekslaboratoriumwetenschapper achteloos culturen van levende moicroben in de afvoer giet?
- Een groep cellen wordt een cel genoemd?
- In welke eiwitten worden afgebroken?
- Welk deel van een cel assembleert eiwitten bij organellen?
- Wat verlaagt de pH-waarde bij mensen?
- Wetenschappers creëren synthetisch prototype dat in staat is om gesynchroniseerd te kloppen
- Waarom bepaalde ijsjes bestand zijn tegen smelten:een wetenschappelijke verklaring

- Op Mars of de aarde, biohybride kan koolstofdioxide omzetten in nieuwe producten

- Onderzoekers komen dichter bij auto's op waterstof
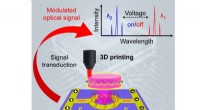
- Nieuw record:3D-geprinte optisch-elektronische integratie
 Wat zijn de belangrijkste ingredanten van de bodem?
Wat zijn de belangrijkste ingredanten van de bodem?  Satellietgegevens verzamelen die Australië wil:een nieuwe richting voor aardobservatie
Satellietgegevens verzamelen die Australië wil:een nieuwe richting voor aardobservatie Wat is de constante energie -eis?
Wat is de constante energie -eis?  Wat is het voordeel van zonne -energie in vergelijking met andere bronnen?
Wat is het voordeel van zonne -energie in vergelijking met andere bronnen?  Waarom het laten ontsnappen van zalm gunstig zou kunnen zijn voor beren en vissers
Waarom het laten ontsnappen van zalm gunstig zou kunnen zijn voor beren en vissers  Wat is de oplosbaarheid van natriumchloride bij kamertemperatuur?
Wat is de oplosbaarheid van natriumchloride bij kamertemperatuur?  Wat is een voorbeeld van potetiale energie?
Wat is een voorbeeld van potetiale energie?  Wat zijn de vijf klassen van immunoglobulinen?
Wat zijn de vijf klassen van immunoglobulinen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

