
Wetenschap
Vloeistoffen versus gassen:de moleculaire structuur en eigenschappen begrijpen
Hier is een overzicht:
* Vloeistoffen: De moleculen in een vloeistof liggen dicht bij elkaar, maar kunnen om elkaar heen bewegen. Ze hebben een vast volume, maar geen vaste vorm.
* Gassen: De moleculen in een gas bevinden zich ver uit elkaar en bewegen zich vrij in alle richtingen. Ze hebben geen vast volume of vorm.
Belangrijkste verschillen:
* Spatiëring: Moleculen in vloeistoffen zitten dichter bij elkaar dan in gassen.
* Beweging: Moleculen in vloeistoffen bewegen vrijer dan in vaste stoffen, maar minder vrij dan in gassen.
* Vorm: Vloeistoffen nemen de vorm aan van hun container, terwijl gassen de hele container waarin ze zich bevinden vullen.
Voorbeeld:
* Water (vloeistof): Watermoleculen bevinden zich dicht bij elkaar, maar kunnen zich verplaatsen, waardoor het kan stromen.
* Lucht (gas): Luchtmoleculen bevinden zich ver uit elkaar en bewegen vrij, waardoor lucht samendrukbaar wordt.
Belangrijke opmerking: Hoewel we het vaak hebben over vloeistoffen en gassen die uit moleculen bestaan, zijn er enkele stoffen (zoals elementaire metalen zoals kwik) die bij kamertemperatuur als vloeistoffen bestaan, ook al is hun structuur niet gebaseerd op individuele moleculen.
 Kun je de oorzaak en het effect vertellen van we geïrrigeerd zodat maïs lang werd?
Kun je de oorzaak en het effect vertellen van we geïrrigeerd zodat maïs lang werd?  Hoeveel zaad eten vogels per dag?
Hoeveel zaad eten vogels per dag?  What will happen if there is same climate on the earth?
What will happen if there is same climate on the earth?  Feedbacklus betekent dat de gevolgen van bosbranden voor de gezondheid waarschijnlijk ernstiger zullen zijn door klimaatverandering
Feedbacklus betekent dat de gevolgen van bosbranden voor de gezondheid waarschijnlijk ernstiger zullen zijn door klimaatverandering Dieren in de Middellandse Zee
Dieren in de Middellandse Zee
Hoofdlijnen
- Studie onthult hoe moleculaire parasieten zich vermenigvuldigen en het vermogen verspreiden om ziekten te veroorzaken
- Hoe definieer je orgel?
- Wat is de wetenschappelijke notatie van een bij?
- Waarom moet de cel zijn DNA voor mitose repliceren?
- Does bacteria grow in cooked rice?
- Nucleotide -subeenheid gemaakt van ribosesuikeradenine en fosfaten die transport opslaan?
- Welke technologie was nodig voordat de celtheorie zich ontwikkelde?
- Onderzoek naar de pijlers van de microbiologie:domeinen, groepen, disciplines en kernactiviteiten
- Welke organismen zijn afhankelijk van andere voor voedsel?
- Duurzaam bouwen met milieuvriendelijk beton

- Unieke nieuwe antivirale behandeling gemaakt met suiker
- Team haalt inspiratie uit natuurlijke wonderen om nieuwe materialen te maken

- Onderzoekers vinden waarde in ongebruikelijk type plantmateriaal

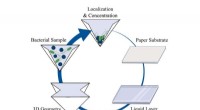
- Gevouwen papier creëert een draagbaar laboratorium voor veldlaboratoriumtests
 Wat is de tegenstelling tussen continentale drift en het verspreiden van vloeren?
Wat is de tegenstelling tussen continentale drift en het verspreiden van vloeren?  Stikstof verminderen met boor en bier
Stikstof verminderen met boor en bier Hoeveel centimeter zijn er op 2 meter?
Hoeveel centimeter zijn er op 2 meter?  De luchtdruk wordt lager naarmate er watermoleculen aan de lucht worden toegevoegd, omdat .?
De luchtdruk wordt lager naarmate er watermoleculen aan de lucht worden toegevoegd, omdat .?  Wie heeft de grafietanode vermoord? Onderzoekers brengen de li-ionbatterijtechnologie met siliciumanode vooruit
Wie heeft de grafietanode vermoord? Onderzoekers brengen de li-ionbatterijtechnologie met siliciumanode vooruit  Hoe kan statische elektriciteit op een object opbouwen?
Hoe kan statische elektriciteit op een object opbouwen?  Topologische nano-elektronica
Topologische nano-elektronica Wat gebeurt er bij een turbine tijdens de elektriciteitsproductie?
Wat gebeurt er bij een turbine tijdens de elektriciteitsproductie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

