
Wetenschap
Covalente obligaties versus ionen:het verschil begrijpen
* Covalente obligaties: In een covalente binding delen atomen elektronen om een stabiele elektronenconfiguratie te bereiken. Ze dragen elektronen niet volledig over, zoals bij ionische bindingen.
* Ionen: Ionen worden gevormd wanneer een atoom elektronen wint of verliest, wat resulteert in een netto positieve of negatieve lading.
Dit is het belangrijkste verschil:
* Ionische bindingen: Betrek de volledige overdracht van elektronen, waardoor positief geladen kationen en negatief geladen anionen ontstaan.
* Covalente bindingen: Betrek het delen van elektronen tussen atomen. De gedeelde elektronen worden aangetrokken door de kernen van beide atomen en houden ze bij elkaar.
Voorbeeld:
* Ionische binding: Natriumchloride (NaCl). Natrium verliest een elektron om een positief geladen natriumion (Na+) te worden, terwijl chloor een elektron krijgt om een negatief geladen chloride-ion (Cl-) te worden. De elektrostatische aantrekkingskracht tussen deze tegengesteld geladen ionen vormt de ionische binding.
* Covalente binding: Water (H2O). Elk waterstofatoom deelt een elektron met het zuurstofatoom, waardoor een stabiel molecuul zonder ionen ontstaat.
Samenvattend gaat het bij covalente bindingen om het delen van elektronen en niet om het delen van elektronen. Er ontstaan dus geen ionen.
 Is de aantrekkingskracht sterker in moleculen een vaste stof of vloeistof?
Is de aantrekkingskracht sterker in moleculen een vaste stof of vloeistof?  Welke maakt geen deel uit van nucleaire chemie?
Welke maakt geen deel uit van nucleaire chemie?  Wat converteert stikstof uit een vorm die kan worden geassimileerd door planten naar N2.
Wat converteert stikstof uit een vorm die kan worden geassimileerd door planten naar N2.  EHBO-kit in sommige levende organismen helpt bij het repareren van DNA na langdurige blootstelling aan de zon
EHBO-kit in sommige levende organismen helpt bij het repareren van DNA na langdurige blootstelling aan de zon Is het gedistilleerd waterelementverbinding of het mengsel?
Is het gedistilleerd waterelementverbinding of het mengsel?
Hoofdlijnen
- Welke cellen verantwoordelijk voor immuniteit?
- Spierreconstructie laat zien hoe dinosaurussen stonden
- Wat zegt de cel in de cyclus?
- Welke organel omzet voedingsstoffen in energie in een dierencel?
- Welk type immuuncellen zitten in de varkensgriep?
- Waarom gebruiken wetenschappers wetenschappelijke namen voor organismen?
- Wanneer kan het vertellen dat plantencellen osmose ondergaan zonder een schaal te gebruiken?
- Wat is de functie OD -kern in dierlijke cellen?
- Hoe ziet en dierencel eruit?
- Beheers de chaos om keramiek met hoge entropie te maken

- Vogelenzym wijst op nieuwe therapieën
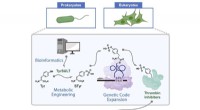
- De radicale manieren waarop zonlicht grotere moleculen in de atmosfeer bouwt
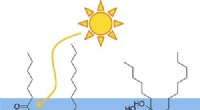
- Onderzoek levert potentiële bioblendstock op voor dieselbrandstof

- Forensisch chemici lasertechniek onderscheidt menselijk en dierlijk bloed

 Wat zijn twee manieren waarop mineralen zich kunnen vormen en hoe ze verschillen?
Wat zijn twee manieren waarop mineralen zich kunnen vormen en hoe ze verschillen?  Hoe wordt energie geconserveerd in het proces van hartslag?
Hoe wordt energie geconserveerd in het proces van hartslag?  Seismische kaart van Noord-Amerika onthult geologische aanwijzingen, aardbeving gevaren
Seismische kaart van Noord-Amerika onthult geologische aanwijzingen, aardbeving gevaren Life Science staat ook bekend als?
Life Science staat ook bekend als?  Nieuwe beeldvormingstechniek legt schoonheid vast van met metaal gelabelde neuronen in 3-D
Nieuwe beeldvormingstechniek legt schoonheid vast van met metaal gelabelde neuronen in 3-D Hoe zuurstof uit vloeibare lucht te scheiden
Hoe zuurstof uit vloeibare lucht te scheiden  Hoe veilig is het GSM Cell Phone Network?
Hoe veilig is het GSM Cell Phone Network?  Wat voor soort vervuiling is er in Ecuador?
Wat voor soort vervuiling is er in Ecuador?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

