
Wetenschap
Benzoëzuur versus natriumchloride:smeltpunten en intermoleculaire krachten vergelijken
* Smeltpunt: Smeltpunt is de temperatuur waarbij een vaste stof in een vloeistof verandert.
* Benzoëzuur heeft een smeltpunt van ongeveer 122,4 °C (252,3 °F).
* Natriumchloride heeft een smeltpunt van 801 °C (1474 °F).
* Intermoleculaire krachten: De kracht van de krachten die moleculen in een vaste stof bij elkaar houden, bepaalt het smeltpunt.
* Benzoëzuur: Vormt waterstofbruggen, die relatief sterk maar zwakker zijn dan ionische bindingen.
* Natriumchloride: Is een ionische verbinding, wat betekent dat het een sterke elektrostatische aantrekkingskracht heeft tussen positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (Cl-).
Conclusie: Omdat natriumchloride veel sterkere ionische bindingen heeft dan de waterstofbruggen in benzoëzuur, vereist het aanzienlijk meer energie (hogere temperatuur) om die bindingen te verbreken en te smelten.
 Een nieuw magnetisch materiaal en opnameproces om de datacapaciteit enorm te vergroten
Een nieuw magnetisch materiaal en opnameproces om de datacapaciteit enorm te vergroten Wat is een trap die is gevormd als twee of meer verschillende soorten atomen combineren?
Wat is een trap die is gevormd als twee of meer verschillende soorten atomen combineren?  Wat is de atoommassa van argon in gram?
Wat is de atoommassa van argon in gram?  Kan een propaantank exploderen?
Kan een propaantank exploderen?  Wat wordt gevormd wanneer bijtende frisdrank gemengd met olie?
Wat wordt gevormd wanneer bijtende frisdrank gemengd met olie?
 Over hoe het ecologisch evenwicht in detail te behouden?
Over hoe het ecologisch evenwicht in detail te behouden?  Tanzania zegt dat de Kilimanjaro-brand is ingeperkt
Tanzania zegt dat de Kilimanjaro-brand is ingeperkt Ideologie en de overgang naar ecologische duurzaamheid
Ideologie en de overgang naar ecologische duurzaamheid Wat is de fundamentele regel aan de basis van alle elecrische fenomenen?
Wat is de fundamentele regel aan de basis van alle elecrische fenomenen?  Het paradijs herwonnen? Deskundigen roepen op tot een Europese aanpak van de Amerikaanse huizenmarkt
Het paradijs herwonnen? Deskundigen roepen op tot een Europese aanpak van de Amerikaanse huizenmarkt
Hoofdlijnen
- Wat zijn de 4 structuren die alle cellen moeten overleven?
- Giftige mannelijkheid:waarom mannelijke trechterwebspinnen zo gevaarlijk zijn
- Welke evolutionaire gebeurtenis vindt plaats als een soort vertakt?
- Wat is een wetenschappelijk woord dat begint met C?
- Wat is testbare hypothiesis?
- Hoe kunt u biologisch in een zin gebruiken?
- Wat vertrouwt op evolutie door natuurlijke selectie?
- Wat is de actie of beweging van een organisme als resultaatstimulus?
- Waarom worden sekscellen beschouwd als haploïden?
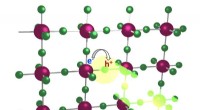
- Organische afstandhouders verbeteren de LED-prestaties
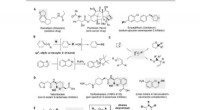
- Invoeging van boor in alkyletherbindingen via tandemkatalyse van zink/nikkel
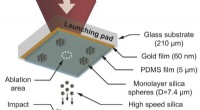
- Onderzoekers laten zien dat materialen vanzelf sterker worden wanneer ze met zeer hoge snelheid worden geraakt
- Een vereenvoudigde methode om olijfolie te categoriseren

- Volledig geïdentificeerd - het pad van protonen

 Wat is de natuurlijke bron van aluminium?
Wat is de natuurlijke bron van aluminium?  Wat legt uit waarom geleiders en isolatorproducten?
Wat legt uit waarom geleiders en isolatorproducten?  Is minder energie nodig voor objecten met een hoge specifieke warmtecapaciteit?
Is minder energie nodig voor objecten met een hoge specifieke warmtecapaciteit?  Hoe The Nature Conservancy werkt
Hoe The Nature Conservancy werkt  Hoe dik is 0,118 inch?
Hoe dik is 0,118 inch?  Hoe rotsen op aarde roestten en rood werden
Hoe rotsen op aarde roestten en rood werden  Team demonstreert kwantumstippen die zichzelf assembleren
Team demonstreert kwantumstippen die zichzelf assembleren Op welke twee dingen hangt warmte van afhankelijk?
Op welke twee dingen hangt warmte van afhankelijk?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

