Wetenschap
Spontane reacties begrijpen bij 298K:Gibbs Free Energy
* ΔG <0: De reactie is spontaan (exergonisch)
* ΔG> 0: De reactie is niet-spontaan (endergoon)
* ΔG =0: De reactie is in evenwicht
De verandering in Gibbs Vrije Energie houdt verband met enthalpieverandering (ΔH) en entropieverandering (ΔS) door de vergelijking:
ΔG =ΔH - TΔS
waar:
* ΔH is de verandering in enthalpie (warmte die vrijkomt of wordt geabsorbeerd)
* T is de temperatuur in Kelvin
* AS is de verandering in entropie (stoornis of willekeur)
Daarom kan een spontane reactie bij 298 K optreden in de volgende scenario's:
1. Exotherme reactie (ΔH <0) met een toename van de entropie (ΔS> 0): Dit scenario resulteert altijd in een negatieve ΔG, waardoor de reactie spontaan wordt.
2. Exotherme reactie (ΔH <0) met een kleine afname van de entropie (ΔS <0): Als de enthalpieverandering significant negatief is, kan deze een kleine afname van de entropie overwinnen, wat leidt tot een negatieve ΔG en een spontane reactie.
3. Endotherme reactie (ΔH> 0) met een grote toename van de entropie (ΔS> 0): Als de entropietoename significant genoeg is om op te wegen tegen de positieve enthalpieverandering, zal de reactie een negatieve ΔG hebben en spontaan zijn.
Voorbeelden van spontane reacties bij 298 K:
* Verbranding van brandstoffen: Exotherm met een grote toename van de entropie.
* Oplossen van keukenzout in water: Endotherm met een grote toename in entropie.
* Neutralisatiereactie van een sterk zuur met een sterke base: Exotherm met een kleine toename in entropie.
Opmerking: De spontaniteit van een reactie kan ook worden beïnvloed door factoren zoals concentratie, druk en de aanwezigheid van katalysatoren.
 Een atoom heeft 11 protonen 13 neutronen en elektronen Wat zijn mogelijk isotopen van dit atoom?
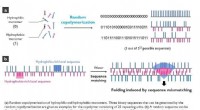
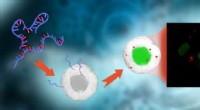
Een atoom heeft 11 protonen 13 neutronen en elektronen Wat zijn mogelijk isotopen van dit atoom?  Van atoom tot natural killer cel:het verhaal van een onverwachte eiwitstructuur
Van atoom tot natural killer cel:het verhaal van een onverwachte eiwitstructuur Welk edelgas is monotoon?
Welk edelgas is monotoon?  Is Uranus meestal gemaakt van gas?
Is Uranus meestal gemaakt van gas?  Hoeveel valentie-elektronen moeten er in de Lewis-structuur voor LiCl worden ondergebracht?
Hoeveel valentie-elektronen moeten er in de Lewis-structuur voor LiCl worden ondergebracht?
 Luchtvervuiling neemt af in Spanje na implementatie van maatregelen ter bestrijding van COVID-19
Luchtvervuiling neemt af in Spanje na implementatie van maatregelen ter bestrijding van COVID-19 Studie van natuurlijke landschappen en fysieke systemen?
Studie van natuurlijke landschappen en fysieke systemen?  Londen, Parijs, Seoul lanceert naam en schande vervuilende auto-index
Londen, Parijs, Seoul lanceert naam en schande vervuilende auto-index Wat zijn de voordelen van biologisch afbreekbaar plastic?
Wat zijn de voordelen van biologisch afbreekbaar plastic?  Drie belangrijke kenmerken van de binnenplaneten
Drie belangrijke kenmerken van de binnenplaneten
Hoofdlijnen
- Wat is differentiatie in de biologie?
- Kun je de biologische klok omkeren?
- Wat is de beste wetenschappelijke ontdekking?
- Hoe worden veel orgelsystemen samengewerkt?
- Welke cellen vormen het epitheelweefsel?
- Wat noemde Gregor Mendel de eigenschappen die verdwijnen in de eerste generatie?
- Wat is het verschil tussen een cel en weefsel?
- Zijn organismen in hetzelfde gezin minder of nauwer verbonden dan bestelling?
- Waarom is de kern een cirkel?
 Veldgevoelige mechanische metamaterialen (FRMM's)
Veldgevoelige mechanische metamaterialen (FRMM's) Waarom denk je dat het weer wordt gebruikt om de afbraak van rotsen te verwijzen?
Waarom denk je dat het weer wordt gebruikt om de afbraak van rotsen te verwijzen?  Een externe gemeenschap heeft wanhopig meer elektrische energie nodig. Het bevindt zich in een gebied met de volgende kenmerken Gemiddelde windsnelheid van 15 en Ndash 20 kmhr Sommige middelgrote rivieren slow-m?
Een externe gemeenschap heeft wanhopig meer elektrische energie nodig. Het bevindt zich in een gebied met de volgende kenmerken Gemiddelde windsnelheid van 15 en Ndash 20 kmhr Sommige middelgrote rivieren slow-m?  Chemicaliën van boerenvelden waar stromen ze niet aan?
Chemicaliën van boerenvelden waar stromen ze niet aan?  Welke lagen van de zon worden alleen gezien tijdens een zonsverduistering?
Welke lagen van de zon worden alleen gezien tijdens een zonsverduistering?  Wat is de functie van een controle in biologische experimenten?
Wat is de functie van een controle in biologische experimenten?  Fycologen ontdekken waardoor sommige bruine algen glinsteren en andere niet
Fycologen ontdekken waardoor sommige bruine algen glinsteren en andere niet  Is geïoniseerd water schadelijk voor mensen met hart illneses?
Is geïoniseerd water schadelijk voor mensen met hart illneses?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com