
Wetenschap
Chemische reacties begrijpen:hoe atomen zich binden
1. Elektronenconfiguratie:
* Valentie-elektronen: De buitenste elektronen in een atoom worden valentie-elektronen genoemd. Zij zijn degenen die betrokken zijn bij chemische binding.
* Octetregel: De meeste atomen streven naar een stabiele elektronenconfiguratie zoals die van een edelgas (groep 18 op het periodiek systeem), dat doorgaans acht elektronen in hun buitenste schil heeft (behalve helium, dat er twee heeft). Dit staat bekend als de octetregel.
2. Elektronegativiteit:
* Elektronegativiteit is de maatstaf voor het vermogen van een atoom om elektronen aan te trekken in een chemische binding.
* Atomen met een hogere elektronegativiteit hebben de neiging elektronen sterker aan te trekken. Dit beïnvloedt het type binding dat wordt gevormd:
* Ionische bindingen: Gevormd wanneer er een groot verschil in elektronegativiteit is tussen twee atomen. Het ene atoom 'doneert' effectief een elektron aan het andere, waardoor ionen ontstaan met tegengestelde ladingen die elkaar aantrekken.
* Covalente obligaties: Gevormd wanneer atomen elektronen delen. Het delen kan gelijk zijn (niet-polaire covalente binding) of ongelijk (polaire covalente binding), afhankelijk van het verschil in elektronegativiteit.
3. Ionisatie-energie:
* Ionisatie-energie is de energie die nodig is om een elektron uit een atoom te verwijderen.
* Atomen met lagere ionisatie-energieën hebben de neiging gemakkelijker elektronen te verliezen, waarbij ze vaak kationen vormen (positief geladen ionen).
4. Elektronenaffiniteit:
* Elektronenaffiniteit is de verandering in energie wanneer een elektron aan een neutraal atoom wordt toegevoegd om een negatief ion (anion) te vormen.
* Atomen met een hoge elektronenaffiniteit nemen gemakkelijk elektronen op.
5. Atoomgrootte:
* Atoomgrootte speelt een rol in hoe gemakkelijk een atoom kan interageren met andere atomen. Grotere atomen hebben meer losjes vastgehouden elektronen, waardoor de kans groter is dat ze bindingen vormen.
6. Andere factoren:
* Nucleaire lading: Het aantal protonen in de kern van een atoom beïnvloedt de aantrekking ervan tot elektronen.
* Afschermingseffect: De binnenste elektronen "beschermen" de buitenste elektronen tegen de volledige nucleaire lading, waardoor ze gemakkelijker te verwijderen zijn.
Samengevat:
De manier waarop atomen reageren is een complex samenspel van deze factoren. Het begrijpen van de elektronenconfiguratie en de eigenschappen zoals elektronegativiteit, ionisatie-energie en elektronenaffiniteit helpt bij het voorspellen van het type binding dat een atoom zal vormen en hoe het zal interageren met andere atomen.
 Wat drijft eronder – en wat niet
Wat drijft eronder – en wat niet  Genomische gegevens vangen koralen op bij soortvorming en aanpassing
Genomische gegevens vangen koralen op bij soortvorming en aanpassing Onderzoek naar ontbossing van narco's koppelt het verlies van tropische bossen in Midden-Amerika aan cocaïne
Onderzoek naar ontbossing van narco's koppelt het verlies van tropische bossen in Midden-Amerika aan cocaïne Welke staat van materie omringt ons allemaal?
Welke staat van materie omringt ons allemaal?  Wat gebeurt er met een regenwoud als het wordt gekapt?
Wat gebeurt er met een regenwoud als het wordt gekapt?
Hoofdlijnen
- Bij mensen is het aantal tetrads gevormd tijdens mitose?
- Wat voor soort spieren zijn langwerpig gerangschikt in vellen en bevatten meerdere kernen?
- Zeehonden en onze kusten
- Is Plantae enkelvoudig cellen of meercellulair?
- Welke genen met verschillende informatie op dezelfde locus?
- Hoe verschillen organismen in het domein Eurkaya van die archaea?
- Wat zijn voorbeelden van niet -vasculaire planten?
- Wat houdt de twee strengen van een DNA -molecuul aan elkaar vast?
- Een mitochondrion heeft een probleem met het creëren van voldoende energie om nieuwe moleculen te bouwen die waarschijnlijk bestaat bij de Mitochondriaan?
- Een belangrijke aanvulling op de toolkit voor scheikundigen voor het bouwen van nieuwe moleculen

- Op palladium gebaseerd metaalglas met hoge trombogene weerstand
- Begrijpen hoe u een mengsel van verbindingen kunt oplossen

- Gemanipuleerde microben kunnen biologisch afbreekbare kunststoffen produceren tegen lagere kosten en milieu-impact dan plantaardige kunststoffen

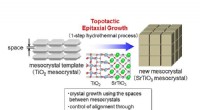
- Fotokatalysator maakt waterstofproductie 10 keer efficiënter
 54 Koolstofatomen Hoeveel kunnen deel uitmaken van glucose?
54 Koolstofatomen Hoeveel kunnen deel uitmaken van glucose?  Hoeveel potentiële energie wint een baceball van 10 N wanneer het wordt opgeheven door M?
Hoeveel potentiële energie wint een baceball van 10 N wanneer het wordt opgeheven door M?  Ontwikkelingslanden moeten hun eigen koers uitstippelen naar netto nulemissie
Ontwikkelingslanden moeten hun eigen koers uitstippelen naar netto nulemissie Wat is de centrale die afval verbrandt om elektriciteit te produceren?
Wat is de centrale die afval verbrandt om elektriciteit te produceren?  Voorheen onbekende dinosaurussoort geïdentificeerd in het zuidwesten van Duitsland
Voorheen onbekende dinosaurussoort geïdentificeerd in het zuidwesten van Duitsland Formules voor het bepalen van de specifieke zwaartekracht
Formules voor het bepalen van de specifieke zwaartekracht Professor stelt voor hoe een zwart gat in een baan rond de planeet een teken zou kunnen zijn van een geavanceerde beschaving
Professor stelt voor hoe een zwart gat in een baan rond de planeet een teken zou kunnen zijn van een geavanceerde beschaving  Hoe noem je de kracht rond een magneet?
Hoe noem je de kracht rond een magneet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

