
Wetenschap
Kookpunten van ester versus carboxylzuur:het verschil begrijpen
1. Gebrek aan waterstofbinding:
* Carboxylzuren vormen sterke waterstofbruggen met elkaar vanwege de aanwezigheid van het zure waterstofatoom. Deze waterstofbruggen vereisen aanzienlijke energie om te breken, wat leidt tot hogere kookpunten.
* Esters missen het zure waterstofatoom, zodat ze alleen zwakke dipool-dipoolinteracties kunnen vormen. Deze interacties zijn veel zwakker dan waterstofbruggen, wat resulteert in lagere kookpunten.
2. Gereduceerde polariteit:
* Carboxylzuren hebben een hogere polariteit dan esters vanwege de aanwezigheid van de polaire hydroxylgroep (-OH). Deze hogere polariteit draagt verder bij aan sterkere intermoleculaire krachten en hogere kookpunten.
* Esters hebben een minder polaire structuur, waarbij het zuurstofatoom in de carbonylgroep (C =O) minder elektronegatief is dan de zuurstof in de hydroxylgroep van carbonzuren. Dit vermindert de sterkte van dipool-dipoolinteracties en resulteert in lagere kookpunten.
3. Moleculair gewicht:
* Hoewel dit niet de voornaamste reden is, is het molecuulgewicht van esters doorgaans iets lager dan dat van de overeenkomstige carbonzuren. Dit kleinere molecuulgewicht draagt enigszins bij aan het lagere kookpunt van esters.
Samengevat:
Het gebrek aan waterstofbinding en de verminderde polariteit in esters in vergelijking met carbonzuren zijn de belangrijkste redenen voor hun lagere kookpunten. Deze factoren verminderen de sterkte van de intermoleculaire krachten aanzienlijk, waardoor het gemakkelijker wordt om esters te verdampen.
 Hoeveel mol ammoniumionen zijn er in 8,754 g carbonaat?
Hoeveel mol ammoniumionen zijn er in 8,754 g carbonaat?  Samengestelde woorden versus samengestelde woorden uit één woord:een duidelijke uitleg
Samengestelde woorden versus samengestelde woorden uit één woord:een duidelijke uitleg  Hoe heet het veranderen van het ene metaal in het andere?
Hoe heet het veranderen van het ene metaal in het andere?  Wat bevat een waterstofatoom dat een elektron heeft verloren?
Wat bevat een waterstofatoom dat een elektron heeft verloren?  Welke isotoop wordt tot op heden vaak gebruikt met vervallen organische materie?
Welke isotoop wordt tot op heden vaak gebruikt met vervallen organische materie?
 NASA's IMERG schat de regen van orkaan Doriërs
NASA's IMERG schat de regen van orkaan Doriërs Kustorkanen over de hele wereld intensiveren sneller, vindt nieuwe studie
Kustorkanen over de hele wereld intensiveren sneller, vindt nieuwe studie  Hoe de neveneffecten van klimaatactie het leven voor iedereen zullen verbeteren
Hoe de neveneffecten van klimaatactie het leven voor iedereen zullen verbeteren Hoe Minnesota's kleine, vervuilde Crow River de Mississippi vertroebelt
Hoe Minnesota's kleine, vervuilde Crow River de Mississippi vertroebelt  Nowcasting strandwaterkwaliteit
Nowcasting strandwaterkwaliteit
Hoofdlijnen
- Hoe IJsland een hoofdrol zou kunnen spelen als duurzame alternatieve eiwitexporteur naar Noord-Europa
- Welke moleculen fungeren als energieopslagmolecuul in de spieren door fosfor te doneren om ATP en ADP opnieuw te synthetiseren?
- Wat zijn overeenkomsten en verschillen tussen mitose meiose?
- Wat zijn 3 onderscheidende kenmerken van Euglenophytes?
- Hoe de lever en de nieren communiceren:hormonen, afvalverwijdering en homeostase
- De vorm van het leven:onderzoek werpt licht op hoe cellen nemen
- Het type organismen dat voedselergie door een gemeenschap overdragen en uiteindelijk eten met andere zijn de?
- Wat voor soort plant is de koraalboon?
- Wat is het verschil tussen een gen en eigenschap?
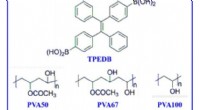
- Grootschalige bereiding van op polymeer gebaseerde fosforescentie bij kamertemperatuur via klikchemie
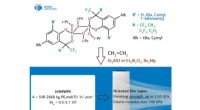
- Een onderzoek naar katalysatoren voor het synthetiseren van polyethyleen met ultrahoog molecuulgewicht
- Onderzoek naar schone lucht zet giftige luchtverontreinigende stoffen om in industriële chemicaliën

- Ultragevoelige transistor voor detectie van herbiciden in water

- Leveren van duurzaam geproduceerde bouwstenen van biomateriaal uit plantaardige grondstoffen

 Is een ei biotisch of abiotisch?
Is een ei biotisch of abiotisch?  Wat betekent het om heterozygoot te zijn voor een eigenschap?
Wat betekent het om heterozygoot te zijn voor een eigenschap?  Wat is een kracht die op alle objecten handelt?
Wat is een kracht die op alle objecten handelt?  Meet het wattage nauwkeurig met een multimeter:een stapsgewijze handleiding
Meet het wattage nauwkeurig met een multimeter:een stapsgewijze handleiding  Hoe koppel op een as
Hoe koppel op een as Filippijnse Everest-veroveraar zet koers naar China
Filippijnse Everest-veroveraar zet koers naar China Dezelfde soort, verschillende maten:zeldzame evolutie in actie gespot bij eilandvleermuizen
Dezelfde soort, verschillende maten:zeldzame evolutie in actie gespot bij eilandvleermuizen  Hoe noem je planten met dikke vlezige weefsels?
Hoe noem je planten met dikke vlezige weefsels?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

