
Wetenschap
Magnesium en zuurstof:de vorming van ionische bindingen begrijpen
* Elektronegativiteit: Elektronegativiteit is het vermogen van een atoom om elektronen naar zich toe te trekken in een chemische binding. Zuurstof heeft een hoge elektronegativiteit (3,44), terwijl magnesium een lage elektronegativiteit heeft (1,31).
* Elektronenoverdracht: Het grote elektronegativiteitsverschil betekent dat zuurstof een veel sterkere aantrekkingskracht op elektronen heeft dan magnesium. Wanneer ze op elkaar inwerken, "steelt" zuurstof effectief twee elektronen uit magnesium.
* Vorming van ionen: Magnesium, dat twee elektronen heeft verloren, wordt een positief geladen ion (Mg²⁺). Zuurstof, die twee elektronen heeft gekregen, wordt een negatief geladen ion (O²⁻).
* Elektrostatische aantrekkingskracht: Deze tegengesteld geladen ionen worden vervolgens bij elkaar gehouden door een sterke elektrostatische aantrekkingskracht, waardoor de ionische binding wordt gevormd die magnesiumoxide (MgO) vormt.
Samengevat: Het aanzienlijke elektronegativiteitsverschil tussen magnesium en zuurstof drijft de overdracht van elektronen aan, wat leidt tot de vorming van geladen ionen en de elektrostatische aantrekkingskracht die een ionische binding definieert.
 NASA volgt tropische storm Franklin
NASA volgt tropische storm Franklin Sommige zeespiegels in het verleden waren misschien niet zo hoog als gedacht, zegt studie van stijgende en dalende landmassa's
Sommige zeespiegels in het verleden waren misschien niet zo hoog als gedacht, zegt studie van stijgende en dalende landmassa's Wereldlanden nemen plan aan voor een planeet zonder vervuiling
Wereldlanden nemen plan aan voor een planeet zonder vervuiling Wat dieren graven in de grond
Wat dieren graven in de grond  Van materiële schade tot verloren productie:hoe natuurrampen de economie beïnvloeden
Van materiële schade tot verloren productie:hoe natuurrampen de economie beïnvloeden
Hoofdlijnen
- Welk organisme gebruikt pepton en geen glucose tijdens hydrolyse?
- Hoe vertoont het gedrag van het organisme een opkomende eigenschap van de fysiologie van het organisme?
- Hoe leidde een begrip van genetica tot de moderne synthese?
- Wat is het verschil tussen celtheorie en atomaire theorie?
- Hoe de evolutie van vogels snuiten verruilde voor snavels
- Welk stadium van de celcycluscellen verdeelt de kern?
- Wat is de wetenschappelijke naam van thermofielen?
- Dit is de naam van een organisme met twee verschillende allelen?
- Koolhydraten:de meest overvloedige organische verbindingen op aarde
- Grenzen geen barrière voor thermo-elektriciteit
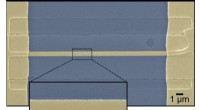
- Aan koude aangepaste enzymen kunnen bij kamertemperatuur transformeren

- Nieuwe aanpak suggereert pad naar emissievrij cement

- Door de spiegel:nieuwe spiegelbeeldmoleculen kunnen leiden tot betere medicijnen
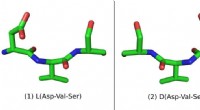
- Het doorbreken van de mal:een ongebruikelijke materiaalkeuze levert batterijen met een ongelooflijk lange levensduur op

 Welke kleur is Neptunes Sky?
Welke kleur is Neptunes Sky?  Wat ontdekten Neil Armstrong en zijn team over de maan?
Wat ontdekten Neil Armstrong en zijn team over de maan?  Hoe kan biotechnologie uw leven beïnvloeden?
Hoe kan biotechnologie uw leven beïnvloeden?  Hoe procent omzetten in decimal
Hoe procent omzetten in decimal Genetisch manipulatiemechanisme gevisualiseerd
Genetisch manipulatiemechanisme gevisualiseerd Wat zijn enkele nadelen over het gebruik van zonne -energie?
Wat zijn enkele nadelen over het gebruik van zonne -energie?  Enorme barrière houdt plastic afval niet vast in de Stille Oceaan
Enorme barrière houdt plastic afval niet vast in de Stille Oceaan Wat is de wetenschappelijke eenheid voor stroom?
Wat is de wetenschappelijke eenheid voor stroom?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

