
Wetenschap
Zuurstofverbindingen:onderzoek naar veel voorkomende chemische combinaties
Zuurstof kan echter verbindingen vormen met andere elementen. Hier zijn enkele veelvoorkomende voorbeelden:
* Water (H₂O): Twee waterstofatomen gebonden aan één zuurstofatoom.
* Kooldioxide (CO₂): Eén koolstofatoom gebonden aan twee zuurstofatomen.
* IJzeroxide (Fe₂O₃): Dit staat algemeen bekend als roest en ontstaat wanneer ijzer reageert met zuurstof.
* Siliciumdioxide (SiO₂): Het hoofdbestanddeel van zand en glas.
* Ozon (O₃): Een molecuul met drie zuurstofatomen.
* Zuurstofrijke koolwaterstoffen: Dit zijn organische verbindingen die naast koolstof en waterstof ook zuurstof bevatten. Voorbeelden hiervan zijn alcoholen (zoals ethanol), ketonen (zoals aceton) en aldehyden (zoals formaldehyde).
Dit is slechts een kleine selectie van de vele verbindingen die zuurstof vormt. Zuurstof is een zeer reactief element en kan gemakkelijk met andere elementen worden gecombineerd om een breed scala aan verbindingen te creëren.
 Patroonanalyses suggereren dat het mogelijk is om vanaf het begin de minimale aardbevingsgrootte te voorspellen
Patroonanalyses suggereren dat het mogelijk is om vanaf het begin de minimale aardbevingsgrootte te voorspellen Wat is het klimaat van Joshua Tree National Park?
Wat is het klimaat van Joshua Tree National Park?  NASA infrarood oog analyseert tyfoon Lingling
NASA infrarood oog analyseert tyfoon Lingling Duizenden geëvacueerd in India nu sterke cycloon steeds dichterbij komt
Duizenden geëvacueerd in India nu sterke cycloon steeds dichterbij komt Wetenschapper test nieuwe technologie voor het verwijderen, voor altijd chemicaliën vernietigen
Wetenschapper test nieuwe technologie voor het verwijderen, voor altijd chemicaliën vernietigen
Hoofdlijnen
- Wat is het verschil tussen prokaryotische en eukaryotische cellen?
- Wanneer voeren dierencellen cellulaire ademhaling uit?
- Kun je mij een zin geven waarin het woord celmembraan wordt gebruikt?
- Plantencellen zijn groen en dier is dit niet omdat alleen plant wat bevat?
- Onderzoek werpt licht op hoe planten aan hun stikstoffixatie komen
- Wat hebben andere organismen die prokaryoten
- Is het waar dat weefsels groepen vergelijkbare cellen zijn, een specifieke functie uitvoeren in een organisme?
- Welke soorten weefsels vormen het skeletsysteem?
- Eén type plantenorganen wordt vegetatieve organen genoemd, wat hebben ze opgenomen?
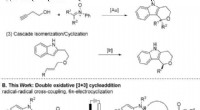
- Onderzoekers onthullen spannende nieuwe manier om farmaceutische ingrediënten goedkoper en veiliger te produceren
- AlScN – alternatief materiaal voor efficiëntere smartphonehardware

- Onderzoekers maken leerachtig materiaal van zijde-eiwitten

- Kunstmest gemaakt van urine kan ruimtelandbouw mogelijk maken

- Malariapathogeen onder de röntgenmicroscoop
 Wat zijn enkele nadelen van het gebruik van de wind als bron voor het genereren van elektriciteit?
Wat zijn enkele nadelen van het gebruik van de wind als bron voor het genereren van elektriciteit?  Hoeveel chromosomen zijn er in cellen gevormd tijdens mitose?
Hoeveel chromosomen zijn er in cellen gevormd tijdens mitose?  Wat creëerden de eerste stervende sterren?
Wat creëerden de eerste stervende sterren?  Wat is een veel voorkomend gebruik van mechanische energie?
Wat is een veel voorkomend gebruik van mechanische energie?  Wat is een transversale golf geproduceerd door de beweging van elektronisch geladen deeltjes?
Wat is een transversale golf geproduceerd door de beweging van elektronisch geladen deeltjes?  Tijdens welk proces vormen gassen de oplossing die u ademt?
Tijdens welk proces vormen gassen de oplossing die u ademt?  Onhandelbare pijn kan verlichting vinden in kleine gouden staafjes
Onhandelbare pijn kan verlichting vinden in kleine gouden staafjes Wat is de dichtheid van acrylplastic in Engelse eenheden?
Wat is de dichtheid van acrylplastic in Engelse eenheden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

