
Wetenschap
Inzicht in atomaire stabiliteit:elektronenschillen en nucleaire balans
* Het heeft een volledige buitenste elektronenschil: Dit is de meest voorkomende en belangrijkste factor. Atomen streven naar een stabiele configuratie met een volledige buitenste schil van elektronen, zoals de edelgassen. Dit betekent dat het het maximale aantal elektronen heeft dat zijn buitenste energieniveau kan bevatten.
* De kern is stabiel: Dit verwijst naar het evenwicht tussen protonen en neutronen in de kern. Te veel of te weinig neutronen kunnen de kern instabiel maken, wat leidt tot radioactief verval.
* Het heeft een lage energiestatus: Atomen streven van nature naar de laagst mogelijke energietoestand. Wanneer een atoom een volledige buitenschil en een stabiele kern heeft, bevindt het zich in een relatief lage energietoestand.
Hier is een overzicht:
* Volledige buitenschaal: Het buitenste energieniveau van een atoom bevat elektronen die deelnemen aan chemische bindingen. Atomen met een volledige buitenste schil (zoals Helium, Neon, Argon) zijn zeer reactief omdat ze al stabiel zijn.
* Stabiele kern: De kern van een atoom bestaat uit protonen (positief geladen) en neutronen (geen lading). De sterke kernkracht houdt deze deeltjes bij elkaar. Als de verhouding tussen protonen en neutronen niet in evenwicht is, kan de kern instabiel worden en vervallen, waardoor energie vrijkomt.
* Lage energiestatus: Stabiele atomen hebben een lage energietoestand. Atomen met een onvolledige buitenste schil of een onstabiele kern hebben doorgaans een hogere energietoestand. Ze zullen reageren of radioactief verval ondergaan om een lagere energietoestand te bereiken.
Samengevat: Stabiele atomen zijn atomen met een volledige buitenste schil van elektronen en een stabiele kern, en bevinden zich in een lage energietoestand. Dit betekent dat het niet waarschijnlijk is dat ze chemische reacties of radioactief verval zullen ondergaan.
 Wat is een sulfide -mineraal met lange metalen slanke blade -kristallen?
Wat is een sulfide -mineraal met lange metalen slanke blade -kristallen?  Het proces van een vloeistof die gas wordt?
Het proces van een vloeistof die gas wordt?  Wat voor soort materialen zou koolstofdioxide beïnvloeden?
Wat voor soort materialen zou koolstofdioxide beïnvloeden?  Wanneer de moleculen in een lichaam met verhoogde snelheid bewegen, is het mogelijk dat van gas naar vloeibaar of vast gas verandert?
Wanneer de moleculen in een lichaam met verhoogde snelheid bewegen, is het mogelijk dat van gas naar vloeibaar of vast gas verandert?  Hoe te Galvaniseren Pewter
Hoe te Galvaniseren Pewter
 Hoe helpen microscopen uw huidige kennis van levende wezens te ontwikkelen?
Hoe helpen microscopen uw huidige kennis van levende wezens te ontwikkelen?  Aardbeving bij onderwatervulkaan Hawaii schudt Big Island door elkaar
Aardbeving bij onderwatervulkaan Hawaii schudt Big Island door elkaar Wetenschappers stellen een nieuwe methode voor om de ongrijpbare oorsprong van CO₂-uitstoot uit stromen te volgen
Wetenschappers stellen een nieuwe methode voor om de ongrijpbare oorsprong van CO₂-uitstoot uit stromen te volgen  Rode tij-opleving spoort ademhalingswaarschuwing op de stranden van Florida aan
Rode tij-opleving spoort ademhalingswaarschuwing op de stranden van Florida aan Koele verfcoatings zorgen ervoor dat voetgangers zich in een stedelijke omgeving tot 1,5°C koeler voelen, zo blijkt uit veldonderzoek
Koele verfcoatings zorgen ervoor dat voetgangers zich in een stedelijke omgeving tot 1,5°C koeler voelen, zo blijkt uit veldonderzoek
Hoofdlijnen
- Wat is het deel van het DNA -molecuul dat informatie bevat voor het maken van 1 eiwit?
- Zijn de subeenheden van een celfunctie onafhankelijk?
- Waarom uw organen snel beginnen te verouderen na 50 jaar
- Kleine genen van zeedieren werpen licht op de evolutie van immuniteit
- Welke plant heeft geen stengel?
- Britse rundvleesboeren willen overstappen naar netto nul, maar praktische en financiële belemmeringen staan in de weg
- Welke term verwijst naar de fasen die een organisme doorloopt vanaf de geboortedood?
- Wat zijn twee belangrijke doelen van het Human Genome Project?
- Zijn de namen die Carolus Linnaeus vandaag nog steeds organismen gaf?
- Arrhenius-zuren uitgelegd:hun dissociatie in water en chemische betekenis

- De nieuwe analysemethode in een record high-speed DNA-assayapparaat

- Van kantoorramen tot Mars:wetenschappers debuteren superisolerende gel

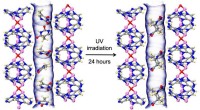
- Nieuwe, door licht aangedreven katalysatoren kunnen helpen bij de productie

- Nieuw biologisch afgeleid metaal-organisch raamwerk bootst DNA na
 Wat is de ijdele stap in cellulaire ademhaling?
Wat is de ijdele stap in cellulaire ademhaling?  Afbeelding:Hertz-kamer voor radiofrequentietesten
Afbeelding:Hertz-kamer voor radiofrequentietesten Wat zijn PUS -cellen?
Wat zijn PUS -cellen?  Hoe dragen de messen op een windturbine bij aan energieverandering?
Hoe dragen de messen op een windturbine bij aan energieverandering?  Penny wise en pound foolish? Het budget van NYC moet rekening houden met de onderlinge verbondenheid van de infrastructuur van de stad
Penny wise en pound foolish? Het budget van NYC moet rekening houden met de onderlinge verbondenheid van de infrastructuur van de stad Welke formatie treedt op wanneer een deel van de korst in een lange lijn wordt verlaagd?
Welke formatie treedt op wanneer een deel van de korst in een lange lijn wordt verlaagd?  Hoe lang duurt het voordat Mercurius de maan draait?
Hoe lang duurt het voordat Mercurius de maan draait?  Mensen betalen om te stemmen kan averechts werken
Mensen betalen om te stemmen kan averechts werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

