
Wetenschap
Ionische verbindingen in water:voorbij H+ en OH-
Zouten:
* Natriumchloride (NaCl): Lost op in Na+ (natriumionen) en Cl- (chloride-ionen).
* Kaliumnitraat (KNO3): Lost op in K+ (kaliumionen) en NO3- (nitraationen).
* Calciumcarbonaat (CaCO3): Lost enigszins op en vormt Ca2+ (calciumionen) en CO32- (carbonaationen).
Zuren (anders dan sterke zuren zoals HCl, HNO3, H2SO4):
* Azijnzuur (CH3COOH): Ioniseert gedeeltelijk en vormt H+ (hydroniumionen) en CH3COO- (acetaationen).
* Koolzuur (H2CO3): Ioniseert en vormt H+ (hydroniumionen) en HCO3- (bicarbonaationen).
Bases (anders dan sterke basen zoals NaOH, KOH):
* Ammoniak (NH3): Reageert met water en vormt NH4+ (ammoniumionen) en OH- (hydroxide-ionen).
Andere ionische verbindingen:
* Magnesiumsulfaat (MgSO4): Lost op in Mg2+ (magnesiumionen) en SO42- (sulfaationen).
* Koper(II)chloride (CuCl2): Lost op in Cu2+ (koper(II)-ionen) en Cl- (chloride-ionen).
Belangrijke opmerking: De mate van ionisatie is afhankelijk van de specifieke stof en de concentratie ervan. Sommige stoffen zijn sterke elektrolyten en ioniseren volledig in water, terwijl andere zwakke elektrolyten zijn en slechts gedeeltelijk ioniseren.
 Is ons fosforgebruik duurzaam? De meeste belanghebbenden betwijfelen dit
Is ons fosforgebruik duurzaam? De meeste belanghebbenden betwijfelen dit  Mens-tijgerconflict:worden de risico’s overschat?
Mens-tijgerconflict:worden de risico’s overschat?  Spanje eert onderzoek naar rol van planten tegen klimaatverandering
Spanje eert onderzoek naar rol van planten tegen klimaatverandering Tropische regenwoudplanten voor kinderen
Tropische regenwoudplanten voor kinderen Spekboomstruiken beschermen de aarde, maar kunnen ze de aarde afkoelen?
Spekboomstruiken beschermen de aarde, maar kunnen ze de aarde afkoelen?
Hoofdlijnen
- Wat is het product van cellulaire ademhaling in termen van belang?
- Een groep organismen die nakomelingen produceren zoals zijzelf?
- De wetenschap zegt:wat er gebeurt als onderzoekers fouten maken
- Is in een wetenschappelijk experimentbeheersing daarvan het onderdeel?
- Ecologische hiërarchie:van biomen tot organismen - een gestructureerd overzicht
- Gewonde zeeschildpad? Print gewoon een spalk!
- Hoeveel chromosomen zitten er in een menselijke eiercel?
- Wat zijn 2 kenmerken van stoffen die hen niet toestaan om door semipermeabele membranen levende cellen te passeren?
- Hoe niet-spiercellen de kracht vinden om te bewegen
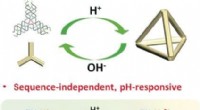
- Universele pH-gereguleerde assemblage van DNA-nanostructuren
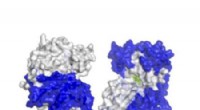
- Ontwikkeling van een enzym tegen antibioticaresistente miltvuur
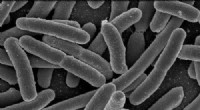
- Een test van 25 minuten kan de eerste diagnose van urineweginfecties vereenvoudigen, strijd tegen antibioticaresistentie
- Een doorbraak in katalysatoren:kleiner dan nanoschaal

- Een onzichtbaar sleutelgat via transparante elektronica

 Op welke manieren reageren land- en watergebieden anders op gelijke insolatie?
Op welke manieren reageren land- en watergebieden anders op gelijke insolatie?  Oorsprong van Cu-Pb-Zn-dragende en W-dragende graniet
Oorsprong van Cu-Pb-Zn-dragende en W-dragende graniet Sociale media voor seksuele voorlichting:Zuid-Afrikaanse tieners leggen uit hoe het hen zou helpen
Sociale media voor seksuele voorlichting:Zuid-Afrikaanse tieners leggen uit hoe het hen zou helpen  Hoeveel pond is 108 gram gelijk?
Hoeveel pond is 108 gram gelijk?  Inzicht in de elektronenrangschikking in covalente bindingen:een uitgebreide gids
Inzicht in de elektronenrangschikking in covalente bindingen:een uitgebreide gids  Welke eenheid is werk gemeten in Si Hertz?
Welke eenheid is werk gemeten in Si Hertz?  Komt licht uit de wolk of grond?
Komt licht uit de wolk of grond?  Een zwart gat breken:hoe de EHT-supertelescoop werkt
Een zwart gat breken:hoe de EHT-supertelescoop werkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

